Selecionar Região
-
Europe
-
Americas
-
Africa and Middle East
-
Asia Pacific
Arnold Marisa (1), Wisdom Shadrach (1), Kerrie Holohan (1), Abed Alkarem Abu Alhaija (2), Emer Gilligan (3), Jill Sommerville (3), Niall Burke (1) (*) e Tim Yeomans (1)
1 Shannon Applied Biotechnology Centre, Universidade Tecnológica de Munster, V92 CX88 Tralee, Irlanda; [email protected] (WS); [email protected] (TY)
2 Divisão de Biociência Oral, Dublin Dental Hospital, Trinity College Dublin, D02 F859 Dublin, Irlanda
3 WaterWipes UC., Donore Road Industrial Estate, Donore Road, Rathmullan, A92 VX00 Drogheda, Irlanda; [email protected] (EG); [email protected] (JS)
*Correspondência: [email protected]
Editora Acadêmica: Maria Manconi
Submissão recebida: 31 de julho de 2024 / Revisada: 13 de setembro de 2024 / Aceita: 26 de setembro de 2024 / Publicada: 1 de outubro de 2024
Resumo
Uma funcionalidade essencial dos toalhitas de limpeza é sua eficiência na remoção de sujeira e contaminação microbiana da pele para níveis seguros ou não detectáveis, tradicionalmente determinados usando o método gravimétrico, que foi relatado como propenso a erros experimentais. Este estudo avalia a eficiência de um lenço umedecido de limpeza à base de água, WaterWipes® (WaterWipes, UC, Drogheda, Irlanda), para remover matéria fecal sintética (Feclone™, SiliClone Creations LLC, Havertown, PA, Estados Unidos) e Escherichia coli (NCTC 10538) da pele de voluntários, o primeiro usando um dispositivo analítico dérmico chamado câmera Antera 3D™ (Miravex Ltd., Dublin, Irlanda) e o último usando métodos microbiológicos padrão. O Feclone™ foi aplicado nos antebraços dos participantes e a câmera Antera 3D™ capturou imagens detalhadas da superfície da pele antes e depois da limpeza. A abordagem da câmera Antera 3D™ foi considerada eficaz na medição da eficiência da limpeza, com o lenço removendo todos os vestígios detectáveis do Feclone™ aplicado. A área total dos poros (mm2), a contagem dos poros e o volume total dos poros (mm3) nos participantes do teste após a limpeza foram observados como reduzidos em média em 39,05%, 34,39% e 39,98%, respectivamente. O lenço removeu 99,99% da E. coli (NCTC 10538) aplicada, conforme medido usando o método de contagem de placas microbianas. Em conclusão, o método da câmera Antera 3D™ foi observado como eficaz na avaliação da remoção do Feclone™ aplicado topicamente.
Palavras-chave: toalhitas de limpeza; câmera Antera 3D™; Feclone™; WaterWipes®; remoção bacteriana
1. Introdução
Os toalhitas podem ser descritos como agentes de limpeza e são geralmente divididos em lenços secos e úmidos, com o uso de toalhitas aumentando nos últimos anos, especialmente em relação à higiene de bebés e crianças pequenas [ 1 ]. Estudos mostram que o uso de toalhitas melhora os resultados da limpeza de fraldas de bebés, oferecendo limpeza eficiente e redução do eritema da pele, adequado para superfícies de pele intactas e danificadas quando comparado ao uso de água e pano [ 2 , 3 , 4 , 5 ]. Os toalhitas para bebés geralmente consistem em materiais de folha de base formulados com um surfactante de limpeza suave, conservantes e agentes tamponantes de pH. A água é geralmente usada como um componente de base em toalhitas para bebés com o propósito de limpar a pele sensível e resíduos fecais de bebés [ 4 , 6 ]. Foi recomendado por uma mesa redonda europeia que toalhitas projetados principalmente para uso em bebés não devem ter o potencial de causar reações de sensibilidade da pele e devem ser formulados com ingredientes que sejam seguros para uso a longo prazo [ 7 ]. Toalhitas projetados para aplicações de limpeza e desinfecção passam por testes padrão, como testes microbiológicos, eficiência de limpeza, absorção de umidade do lenço e formulação de loção [ 1 ], com eficiência de limpeza tradicionalmente determinada usando métodos gravimétricos de limpeza com lenço (como a técnica de recuperação de chocolate derretido) que foram relatados como propensos a erros experimentais [ 1 , 8 ].
Portanto, este estudo busca projetar e avaliar um novo método não gravimétrico com potencial uso futuro para avaliar a eficiência de limpeza de produtos de limpeza comerciais novos e existentes. O método projetado envolve o uso de uma câmera Antera 3D™ conhecida por sua imagem dérmica em tempo real, com vantagens como a entrega de dados precisos, rápidos e objetivos em diferentes áreas de estudos de pele e avaliação de produtos cosméticos [ 9 , 10 , 11 , 12 ]. A câmera Antera 3D™ (Miravex Ltd., Dublin, Irlanda), sob a Patente Europeia nº 2400890, opera no princípio da iluminação da pele de vários ângulos, com dados da superfície da pele reproduzidos de forma 3D usando software habilitado para computador para interpretar a luz refletida da superfície da pele. Dados relevantes da pele que podem ser gerados com este instrumento incluem contagens de poros da pele, rugas, aspereza e análise de pigmentação [ 13 ]. Os poros da pele desempenham um papel na liberação de sebo, suor e detritos celulares da pele. O tratamento de poros faciais dilatados (com terapias como ultrassom, luz de banda larga, radiofrequência e lasers fracionados não ablativos) tem sido relatado como uma das principais demandas cosméticas [ 14 ].
O método projetado foi avaliado usando WaterWipes® (WaterWipes UC, Drogheda, Irlanda), uma marca comercialmente disponível de toalhitas sem surfactante, feitos com ingredientes mínimos. Sua composição básica compreende materiais fibrosos sem plástico (folhas umedecidas de tecido de renda fiada não tecida 100% viscose). As folhas são umedecidas com água ultrapurificada (99,9%) e extrato de semente de citrus grandis (toranja) 0,1% [ 15 ]. Sua eficiência de limpeza foi testada contra aplicações tópicas de FecloneTM e E. coli em dois ensaios separados com voluntários humanos. FecloneTM (SiliClone Creations LLC, Havertown, PA, Estados Unidos) é uma marca patenteada de material fecal artificial simulado com aplicações relatadas em testes de produtos alimentícios, bem como em toalhitas para incontinência e bebés [ 16 , 17 ]. O método de câmera Antera 3DTM adaptado foi usado para avaliar a eficácia de limpeza de um produto de limpeza específico disponível comercialmente no teste FecloneTM e o método de contagem de placas para o teste E. coli.
2. Materiais e Métodos
2.1. Avaliação da eficiência de limpeza do produto Wipe na remoção de Feclone™
Este estudo foi conduzido com base na aprovação ética do Comitê de Ética em Pesquisa Humana da Universidade Tecnológica de Munster (HREC-FER-24-004) e operado de acordo com a BS EN 1500:2013 [ 1 ]. Os critérios de inclusão para o estudo foram homens e mulheres com mais de 18 anos com pele humana adulta saudável, intacta e não sensível, enquanto os critérios de exclusão foram adultos vulneráveis, queixas de pele, sensibilidade da pele (autorrelatada) ou pele quebrada no antebraço. O painel resultante consistiu em 25 voluntários humanos (18 mulheres e 7 homens); amostras e imagens tiradas foram anonimizadas para os participantes. A faixa etária dos participantes neste estudo foi de 18 a 50 anos. A investigação foi conduzida em um ambiente controlado no Laboratório do Centro de Biotecnologia Aplicada de Shannon (MTU, Kerry, Irlanda) com temperatura ambiente (25 ± 2 °C) e umidade relativa (50 ± 5%).
2.1.1. Preparação de Feclone™
No total, 120 mL de água destilada foram aquecidos a 99 °C em um recipiente coberto; simultaneamente, 40 g de Feclone™ foram pré-aquecidos por 5 min usando uma placa quente. Ao atingir a temperatura desejada, a água aquecida foi cuidadosamente adicionada ao Feclone™ (SiliClone Creations LLC, Havertown, PA, EUA), seguido por agitação completa por aproximadamente 20 s usando uma espátula. A mistura foi então coberta com papel alumínio e incubada a 99 °C por um mínimo de 30 min, com a mistura suavemente agitada após os primeiros 10 min. No final do período de incubação, uma breve agitação final foi realizada antes de aliquotar a solução quente em tubos de 50 mL. Os tubos foram colocados a 4 °C até o uso posterior.
2.1.2. Aplicação de Feclone™ no antebraço humano
Os voluntários sentaram-se com um braço apoiado em uma mesa e com o antebraço exposto e puderam se aclimatar às condições do ambiente por 3 min. O objetivo deste estudo foi determinar a eficiência de limpeza do lenço umedecido, e assim a temperatura da pele foi considerada uma prioridade menor. Dentro de uma seção de 8 × 8 cm, uma área de 4 × 4 cm foi protegida colocando um modelo no antebraço do voluntário. Uma quantidade de 2 g de Feclone™ foi aplicada na área de 4 × 4 cm e espalhada uniformemente usando uma espátula. O procedimento de limpeza envolveu limpar a área contaminada verticalmente e horizontalmente da seguinte forma: da esquerda para a direita com uma superfície de lenço umedecido, seguido da direita para a esquerda com outra superfície de lenço umedecido, depois de cima para baixo com uma superfície de lenço umedecido nova e, finalmente, de baixo para cima usando uma nova superfície de lenço umedecido, tudo da mesma folha.
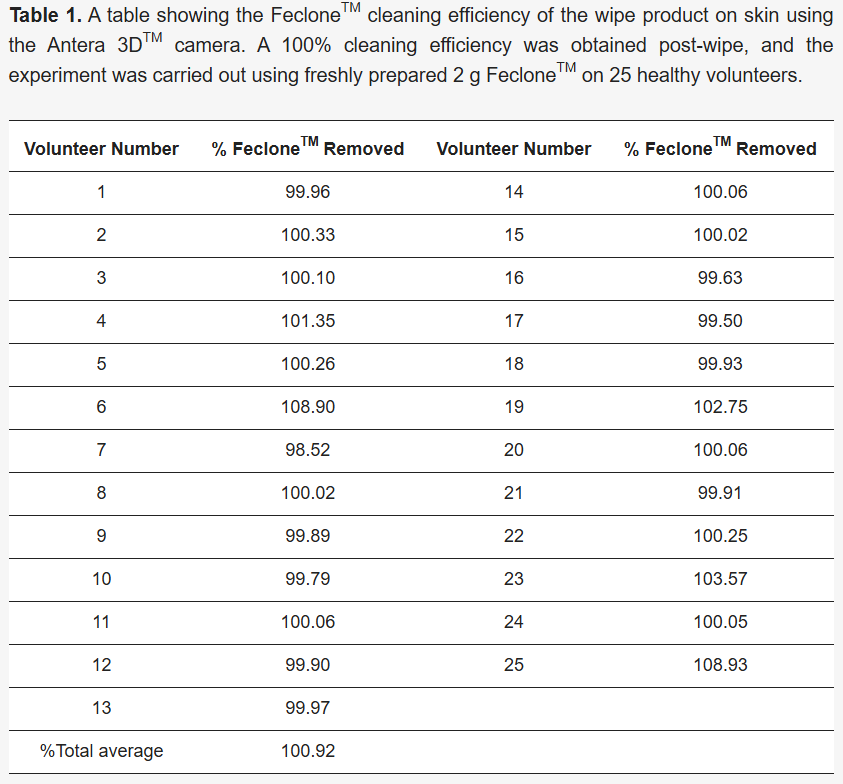
Uma imagem da área marcada foi capturada usando uma câmera Antera 3D™ antes e depois da limpeza, bem como diretamente após a aplicação do Feclone™, e analisada usando o software Antera 3D™ (versão 3.1.8) para comparar as condições pré e pós-limpeza. A porcentagem de remoção foi calculada usando o parâmetro de volume do software, que mede a depressão e a elevação acima de uma superfície de referência normalizada. O volume da pele (mm3) pós-limpeza foi subtraído do volume da pele pré-aplicação do FecloneTM; o valor obtido foi subtraído do volume da pele (mm3) com pré-limpeza com Feclone™ e dividido pelo volume da pele (mm3) com pré-limpeza com Feclone™. Este valor foi então multiplicado por 100 para calcular a porcentagem de remoção (fórmula na Seção 3.1 ) com o resultado obtido encontrado na Seção 3.1 ( Tabela 1 ).
2.2. Avaliação do impacto do produto Wipe nos poros da pele humana
Este estudo foi realizado no antebraço nu de cada voluntário (25 no total). A área de teste foi marcada no braço conforme descrito anteriormente para que as fotos de antes e depois fossem exatamente da mesma área. A área foi então fotografada, seguida por uma aplicação de 2 g de Feclone™. O procedimento de limpeza subsequente foi realizado conforme descrito na Seção 2.1.2 e os resultados obtidos podem ser encontrados na Seção 3.2 ( Tabela 2 ). A fórmula usada para os diferentes parâmetros de poros do software Antera 3D™ (versão 3.1.8) inclui:
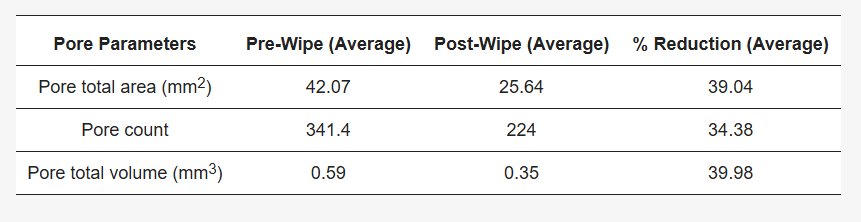
Tabela 2. Uma tabela mostrando o impacto do teste de limpeza nos poros da pele. Os dados foram obtidos e analisados usando o método de câmera Antera 3D™. Uma redução significativa na contagem média de poros, volume e área foi observada após a limpeza em comparação com a imagem pré-limpeza da mesma superfície da pele.
- Volume total de poros (mm3) V = soma da profundidade de cada pixel * área do pixel.
- Área total de poros (mm2) = número de pixels deprimidos * área de pixels.
- Contagem de poros = ilhas de depressão isoladas dentro da região de interesse selecionada.
2.3. Avaliação da eficiência de limpeza do produto Wipe contra E. Coli (NCTC 10538)
Este estudo foi conduzido usando KWIK STIK E. coli (NCTC 10538), meio de cultura bacteriana e 25 voluntários humanos. A preparação do meio de cultura e das culturas iniciais bacterianas foi preparada antes do teste em voluntários.
2.3.1. Cultura bacteriana
No total, 30 g de pó de caldo de soja triptona (TSB) foram adicionados a 100 mL de água destilada. A mistura foi agitada completamente até que o pó estivesse completamente dissolvido. O volume foi então ajustado com água destilada para atingir um volume final de 1 L. Posteriormente, o meio foi esterilizado por autoclavagem. O meio de ágar de soja triptona (TSA) foi preparado de maneira semelhante, mas usando 40 g/L de pó de TSA.
Células de Escherichia coli (E. coli) (NCTC 10538) foram inicialmente inoculadas em placas TSA e então colocadas em uma incubadora ajustada a 37 °C durante a noite. No dia seguinte, uma única colônia foi selecionada e transferida para outra placa TSA, que foi então incubada sob as mesmas condições. No dia subsequente, uma única colônia foi colhida e introduzida em 10 mL de meio TSB. Esta cultura foi incubada durante a noite em temperatura ambiente com agitação. No dia seguinte, a densidade óptica (DO) da cultura foi medida usando um espectrofotômetro, e as células foram diluídas com meio TSB até que uma DO de 0,15 fosse atingida.
2.3.2. Aplicação de bactérias no antebraço de voluntários
Este método foi baseado nas diretrizes descritas na BS EN 1500:2013 [ 1 ]. Culturas de caldo de E. coli com uma densidade óptica (DO) de 0,15 foram consistentemente usadas durante todo o experimento; o número médio de E. coli usado foi de 1,55 × 108 UFC/mL. Uma alíquota desta cultura foi usada para enumeração usando o método de contagem em placa. Os voluntários limparam suas mãos e braços com um sabão não antibacteriano, seguido de esfregaço na área limpa, que foi colocada em 1 mL de meio salino tamponado com fosfato (PBS) para enumeração pelo método de contagem em placa (servindo como controle). Uma área de 4 × 4 cm foi marcada na pele do voluntário para teste. Posteriormente, 100 µL de cultura noturna a DO de 0,15 foram pipetados na área de teste, espalhados suavemente usando um espalhador em forma de L e deixados secar ao ar por 3 min.
Isto foi seguido pelo procedimento de limpeza usando o produto de limpeza conforme descrito na Seção 2.1.2 . A limpeza usada foi então submersa em 10 mL de meio neutralizante Dey-Engley (D3435, Merck, Darmstadt, Alemanha), agitada por 60 s e diluída em série duas vezes com meio PBS. Posteriormente, 0,1 mL da bactéria foi aplicado a uma placa de ágar para cultura durante a noite e quantificação subsequente. Após o processo de limpeza, a superfície da área de teste do antebraço foi esfregada com um cotonete umedecido. O cotonete foi então colocado em 1 mL de meio PBS e 0,1 mL foi aplicado a uma placa de ágar para quantificação. Diluições em série de puro, 10-1 e 10-2 foram aplicadas a uma placa de ágar para quantificação em triplicado. O estoque original de bactérias foi diluído em série a 10−3, 10−4 e 10−5 e semeado em placas de ágar para enumeração de colônias. Para cada área, UFC/mL foi calculado usando a seguinte fórmula:
UFC/mL=(N ∗ DF)/VCFU/mL=(N ∗ DF)/VC
onde UFC/mL = Unidade formadora de colônias por mL:
N = Número de colônias (número total de colônias contadas nas placas dentro da faixa ótima).
DF = Fator de Diluição (o recíproco da diluição usada para o revestimento).
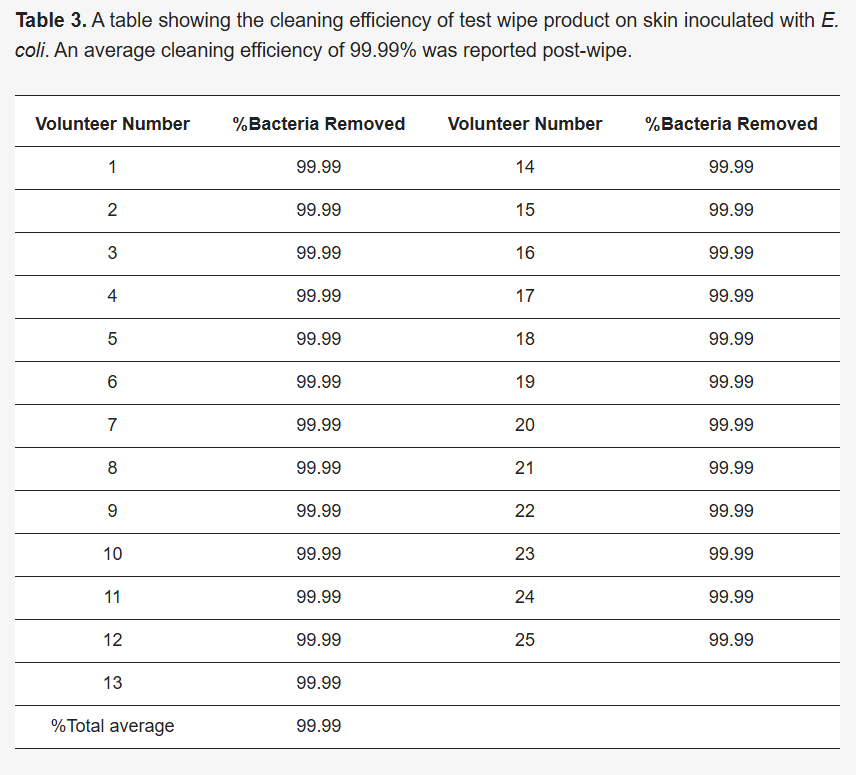
VC = Volume de Cultura Plaqueado (o volume da cultura diluída plaqueada na placa de ágar). A tabela que mostra a porcentagem de bactérias removidas pode ser encontrada na Seção 3.3 ( Tabela 3 ).
3. Resultados
3.1. Avaliação da eficiência de limpeza do produto Wipe na remoção de material fecal simulado (Feclone™)
O método Antera 3D™ adaptado foi usado para avaliar a eficiência de limpeza de lenços de teste em relação à remoção de Feclone™ dos antebraços de voluntários. Os resultados foram analisados usando o parâmetro de volume do software Antera 3D™. O volume se refere à espessura geral ou volume de qualquer resíduo ou contaminante na superfície da pele, e a redução no volume após a limpeza indica remoção bem-sucedida (veja a Figura 1 ). A porcentagem de remoção foi calculada usando a seguinte fórmula:
𝑠𝑣0−𝑠𝑣1⁄𝑠𝑣0×100sv0−sv1∕sv0×100
onde SV0 = Volume de pele (mm3) com pré-limpeza com Feclone™.
SV1 = (Volume de pele (mm3) pós-limpeza - volume de pele (mm3) antes da aplicação de Feclone™).
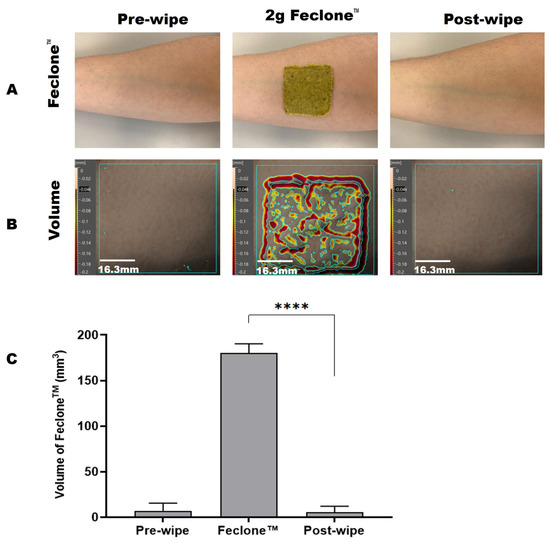
Figura 1. ( A ) Imagens representativas mostrando a pele humana do antebraço antes e depois que Feclone™ foi aplicado e removido usando o produto de teste de limpeza; a imagem foi realizada usando uma câmera de telefone. ( B ) Volume de Feclone™ detectado na superfície da pele do antebraço usando o método Antera 3D™ e limpeza com o produto de limpeza. A área de aplicação para análise foi de 40 mm × 40 mm. A barra de escala vertical representa o volume da pele e a topografia, enquanto a barra de escala horizontal se refere à medição 2D da região definida da pele. ( C ) Mostra os volumes de pele pré-limpeza, Feclone™ e pós-limpeza observados com o método Antera 3DTM. O produto de limpeza foi observado para reduzir o aumento induzido por Feclone™ no volume da pele até os níveis de pré-aplicação. Uma análise de teste t pareado de Feclone™ administrado e volume de pele residual pós-limpeza mostrou uma diferença altamente significativa (**** p < 0,0001). O gráfico foi plotado como média com DP (desvio padrão) usando GraphPad Prism 10 (GraphPad Software, 225 Franklin Street, Fl. 26 Boston, MA 02110, EUA). Isso representa uma eficiência média de limpeza de 100,92%.
3.2. Avaliação do produto Wipe nos poros da pele humana
Foi observada uma redução nos parâmetros dos poros, como contagem total de poros, volume dos poros e área, após a limpeza da pele do antebraço do voluntário com o produto de limpeza ( Figura 2 ).
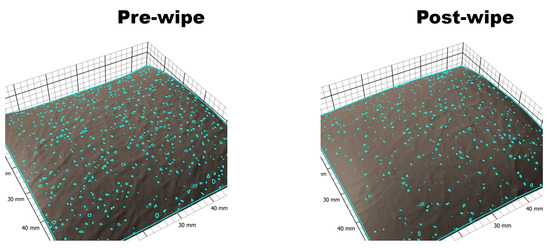
Figura 2. Uma imagem representativa do software Antera 3DTM mostrando a redução observada nos poros detectáveis da pele (contagem, área total, volume total) após a limpeza com produto de limpeza.
3.3. Avaliação da eficiência de limpeza do produto Wipe na remoção de E. Coli
A eficácia do produto de limpeza na remoção de contaminação bacteriana também foi avaliada. O número de UFC/mL foi calculado para cada área, e as médias foram determinadas. Essas descobertas indicam que o produto de limpeza removeu efetivamente 99,99% das células bacterianas e limpou eficientemente as áreas de pele contaminadas. Isso foi validado pela coleta dos lenços usados para quantificação bacteriana após a limpeza, bem como pela limpeza da área limpa para cultura em placas de TSA (veja Figura 3 A,B).
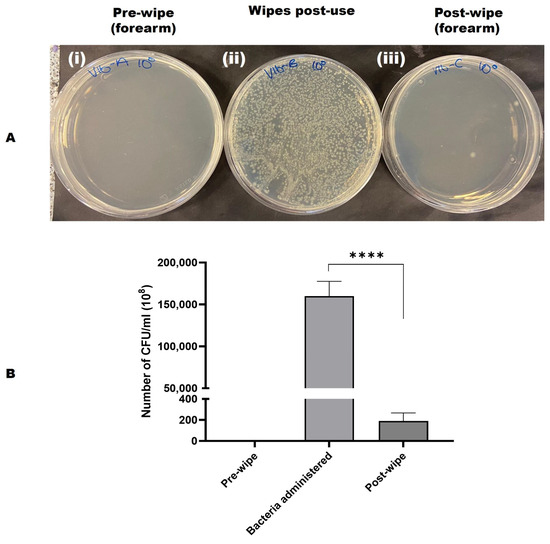
Figura 3. ( A ) Uma imagem representativa mostrando a eficiência de remoção bacteriana de toalhitas de teste de pele humana contaminada. ( i ) Cotonete pré-limpeza banhado ( ii ) Lenço usado banhado ( iii ) Cotonete pós-limpeza banhado. V = voluntário, A = Amostra pré-limpeza, B = Lenço pós-uso, C = Amostra pós-limpeza, 100 = amostra pura/não diluída. ( B ) Gráfico da eficiência de remoção bacteriana do produto de lenço usando E. coli e contagem microbiológica. Observou-se que os toalhitas de teste tiveram 99,99% de remoção de bactérias do que foi administrado. A análise do teste t pareado de bactérias administradas e a contagem pós-limpeza mostraram uma diferença altamente significativa (**** p < 0,0001). O gráfico foi plotado como média com DP (desvio padrão) usando GraphPad Prism 10. V = voluntário, A = Amostra pré-limpeza, B = Lenço pós-uso, C = Amostra pós-limpeza, 100 = amostra pura/não diluída.
4. Discussão
Este estudo teve como objetivo projetar e avaliar um método alternativo para realizar estudos de eficiência de limpeza de produtos de limpeza usando uma câmera Antera 3D™, um dispositivo de imagem dérmica e análise. Toalhitas para bebés disponíveis comercialmente (WaterWipes®) foram usados neste estudo e foram testados quanto à sua eficiência de limpeza com matéria fecal sintética (Feclone™) e E. coli contaminante da superfície da pele dos antebraços de voluntários. A câmera Antera 3D™, uma ferramenta validada de avaliação de produtos cosméticos [ 11 ], tem sido empregada em muitos estudos cosméticos, como aqueles que envolvem a quantificação de rugas, acne e pigmentação [ 11 , 18 , 19 ], e assim uma adaptação do padrão europeu BS EN 1500:2013 [ 1 ] incorporando a câmera Antera 3D™ para avaliação quantitativa e qualitativa da eficiência de limpeza dos toalhitas foi desenvolvida e testada usando o produto de limpeza. A análise objetiva do teste FecloneTM utilizou o parâmetro de volume do software para fornecer uma avaliação aprofundada da eficiência de limpeza dos toalhitas.
Os resultados da avaliação visual e da análise da câmera Antera 3D™ demonstraram que esse método foi apropriado para avaliar a remoção de Feclone™ da pele humana usando toalhitas, que mostraram uma eficiência de limpeza de Feclone™ de 100,92%. Nossa hipótese é que o valor de remoção sendo >100% pode ser devido à sensibilidade do método da câmera Antera 3D™ na detecção da remoção de toalhitas de Feclone™ aplicado e de quaisquer resíduos de pele pré-existentes. Uma abordagem de imagem semelhante para determinar a eficiência de limpeza de toalhitas foi relatada por Lee et al. [ 8 ] e consiste em um computador com um scanner e software de análise de imagem; no entanto, este estudo foi conduzido usando um contaminante espalhado em uma placa de vidro e não em pele humana. As técnicas de imagem, portanto, fornecem uma alternativa ao método gravimétrico tradicional usado para avaliar a eficiência de limpeza de toalhitas, que foi relatado como propenso a erros experimentais.
O método gravimétrico normalmente envolve registrar o peso do lenço antes e depois da limpeza para determinar a eficiência da limpeza. Essa técnica se concentra na análise do lenço e não da superfície que está sendo limpa. O método foi relatado como propenso a erros que podem surgir do processo, como do manuseio dos lenços durante o processo de pesagem, o que pode levar à transferência de umidade do lenço para as luvas do testador e à evaporação inevitável da umidade dos lenços de teste, tudo isso pode afetar os resultados obtidos e deve ser contabilizado como variáveis experimentais. No entanto, com o método da câmera Antera 3D™, que é uma abordagem baseada em óptica, há menos preocupação com a evaporação e o manuseio da umidade do lenço, pois a eficiência da limpeza será deduzida diretamente da superfície da pele e não pela diferença nos pesos dos lenços, tornando esse método potencialmente útil para lidar com erros comuns à análise gravimétrica. Outras vantagens associadas aos métodos propostos da câmera Antera 3D™ incluem sua capacidade de geração de imagens de pele em 3D, facilidade de uso, precisão, reprodutibilidade e sua multileitura para parâmetros de pele, como tamanho de poro, manchas, rugas e aspereza. No entanto, há algumas limitações observadas com os modelos propostos, que incluem incerteza sobre sua aplicabilidade em outras áreas de caracterização da eficiência de toalhitas, como análise da taxa de secagem de toalhitas (taxa de evaporação de umidade do lenço quando exposto à atmosfera ao longo do tempo), análise de coleta de toalhitas (capacidade do úmido de coletar loção) e estudos de transferência de loção (liberação de loção do lenço umedecido para a pele) [ 1 , 8 , 20 ]. Como o método proposto usa um dispositivo específico, a câmera Antera 3D™ e o software associado são necessários para executar ou reproduzir o método, uma limitação potencial de aplicação generalizada. O modelo é uma técnica óptica com variáveis como distância fixa, grau de resolução (0,1 mm) e banda espectral (sete) obtidas com a câmera Antera 3D™, tornando a topografia da pele reconstruída uma estimativa [ 21 ]. A sensibilidade da técnica proposta permite detectar o que está presente na pele (pelos, poros, sebo, cicatrizes, sardas, etc.); no entanto, não se espera que isso influencie ou cause artefatos nos dados gerados, pois o protocolo estabelece que as leituras de linha de base da pele sejam feitas primeiro.
Curiosamente, observou-se que a limpeza da pele com o produto de limpeza em questão teve um impacto na redução da contagem média total de poros, volume e área, e isso é de notável importância, pois vários estudos mostraram uma relação entre uma contagem menor de poros e uma pele mais saudável [ 14 , 22 , 23 ]. Isso provavelmente é atribuído à combinação da formulação e da composição do lenço, em que uma formulação de baixa tensão superficial espalha e molha os poros da pele o suficiente para permitir que o lenço limpe efetivamente os poros de sebo, suor e outros resíduos celulares. A redução na contagem média de poros e tamanho também pode ser auxiliada pela temperatura mais fria dos próprios lenços. A temperatura dos lenços parece mais fria do que a temperatura da pele; portanto, essa pode ser a razão para os poros fecharem temporariamente. Alguns estudos relataram que o resfriamento da pele leva a uma redução no tamanho e na contagem dos poros por meio da vasoconstrição cutânea e do endurecimento da pele [ 24 , 25 , 26 ]. Além disso, o extrato de semente de toranja (GSE), um ingrediente condicionador da pele e um ingrediente no produto de limpeza usado, é relatado como tendo propriedades antimicrobianas [ 27 , 28 , 29 , 30 ]. Também é relatado que possui atividade antioxidante e ajuda a aliviar a congestão da pele ao purificar, limpar e desobstruir os poros obstruídos da pele para uma pele lisa e radiante, bem como fechar os poros da pele devido à sua capacidade matificante [ 31 , 32 ]. É proposto que esses lenços, WaterWipes® (WaterWipes UC, Drogheda, Irlanda), possam ser usados como uma forma menos invasiva de limpar os poros e minimizar sua aparência, visto que, quando considerados como um todo, a mudança na área, volume e contagem dos poros após a limpeza pode ser uma combinação de todos os motivos acima; no entanto, este é um tópico separado, e mais pesquisas precisam ser realizadas para validar essas descobertas e determinar o mecanismo exato de ação, uma vez que as temperaturas dos toalhitas e da pele dos voluntários não foram levadas em consideração neste estudo. No entanto, os recursos de visualização e medição de poros da câmera Antera 3D™ (Miravex Ltd., Dublin, Irlanda) forneceram uma compreensão adicional do efeito que o produto de lenço umedecido tem na pele.
5. Conclusões
Concluindo, as descobertas deste estudo demonstram que o método de câmera Antera 3D™ pode ser uma técnica alternativa eficaz na avaliação da eficiência de toalhitas de limpeza. Seus benefícios incluem sua simplicidade de uso, reprodutibilidade de dados, luz controlada na área interna da imagem e o fato de ser uma unidade portátil com alta resolução e leitura multiparâmetro. No entanto, como nenhuma comparação foi realizada com outros métodos de avaliação da eficiência de limpeza (como a técnica gravimétrica), esta técnica proposta pretende servir como uma alternativa potencial aos métodos existentes. O produto de lenço usado neste estudo demonstrou ter boa eficiência de limpeza em relação à remoção substancial de Feclone™ e E. coli da pele humana. Pesquisas futuras podem explorar o desempenho dos lenços em diferentes tipos de pele e locais do corpo e sob condições ambientais variadas para ampliar sua aplicabilidade e compreensão da eficiência usando o método desenvolvido. No geral, este estudo contribui com insights valiosos sobre a eficácia do método de câmera Antera 3D™ para medir a eficiência de limpeza de toalhitas de limpeza.
Contribuições do autor
Conceitualização, TY, NB, JS e EG; metodologia, AAAA, AM; KH e NB; Investigação e análise de dados, AM, KH e WS; redação — preparação do rascunho original, WS; redação — revisão e edição, WS, NB, JS, EG e TY; recursos, EG, JS e TY; supervisão, NB e TY; administração e financiamento do projeto, TY, EG e JS Todos os autores leram e concordaram com a versão publicada do manuscrito.
Financiamento
Esta pesquisa recebeu financiamento da WaterWipes UC.
Declaração do Conselho de Revisão Institucional
Este ensaio com voluntários humanos foi conduzido de acordo com a Declaração de Helsinque e aprovado pelo Comitê de Ética em Pesquisa Humana da Universidade Tecnológica de Munster (referência MTU-HREC-FER-24-004). A governança do Comitê de Ética em Pesquisa Humana da Universidade Tecnológica de Munster é conforme descrito na Política de Ética em Pesquisa Humana da Universidade [ 33 ], e se alinha com a Declaração de Política Nacional sobre Garantia da Integridade da Pesquisa na Irlanda (Research Integrity National Forum (2019) [ 34 ]. Toda atividade de pesquisa que envolva humanos como participantes da pesquisa deve passar por uma revisão ética formal, antes do início.
Declaração de Consentimento Informado
Todos os voluntários forneceram consentimento informado por escrito antes de participar deste estudo.
Declaração de disponibilidade de dados
Todos os dados podem ser encontrados neste artigo.
Agradecimentos
Todos os voluntários em ambos os estudos são reconhecidos por seu papel na coleta de dados.
Conflitos de interesse
Os autores Jill Sommerville e Emer Gilligan foram empregados pela empresa WaterWipes UC. Os autores restantes declaram que a pesquisa foi conduzida na ausência de quaisquer relações comerciais ou financeiras que pudessem ser interpretadas como um potencial conflito de interesses.
Referências
- Cheriaa, R.; Boubaker, J. Avaliação da qualidade de lenços umedecidos para bebês. J. Ind. Texto. 2022 , 51, 2124S–2147S. [ Google Scholar ] [ CrossRef ]
- Visscher, M.; Odio, M.; Taylor, T.; White, T.; Sargent, S.; Sluder, L.; Smith, L.; Flower, T.; Mason, B.; Rider, M.; et al. Cuidados com a pele no paciente da UTIN: Efeitos de lenços umedecidos versus pano e água na integridade do estrato córneo. Neonatologia 2009 , 96, 226–234. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Garcia Bartels, N.; Massoudy, L.; Scheufele, R.; Dietz, E.; Proquitté, H.; Wauer, R.; Bertin, C.; Blume-Peytavi, U. Regime padronizado de cuidados com fraldas: Um estudo piloto prospectivo e randomizado sobre a função de barreira da pele e IL-1α epidérmica em recém-nascidos. Pediatr. Dermatol. 2012 , 29, 270–276. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Rodriguez, KJ; Foxenberg, R.; Hoffman, D.; Vongsa, R. A ciência por trás dos lenços umedecidos para a pele infantil: revisão de ingredientes, segurança e eficácia. Pediatr. Dermatol. 2020 , 37, 447–454. [ Google Scholar ] [ CrossRef ]
- Odio, M.; Streicher-Scott, J.; Hansen, RC Lenços umedecidos descartáveis para bebês: eficácia e suavidade da pele. Dermatol. Nurs. 2001 , 13, 107–112, 117–118, 121. [ Google Scholar ]
- Ehretsmann, C.; Adam, R. Tolerância cutânea de lenços umedecidos para bebês por bebês com dermatite atópica e comparação da suavidade do lenço umedecido para bebês e da água na pele infantil. J. Eur. Acad. Dermatol. Venereol. 2001 , 15, 16–21. [ Google Scholar ] [ CrossRef ]
- Blume-Peytavi, U.; Lavender, T.; Jenerowicz, D.; Ryumina, I.; Stalder, J.; Torrelo, A.; Cork, MJ Recomendações de uma Mesa Redonda Europeia sobre Melhores Práticas de Cuidados Saudáveis com a Pele Infantil. Pediatr. Dermatol. 2016 , 33, 311–321. [ Google Scholar ] [ CrossRef ]
- Lee, J.; Kim, S.; Oh, KW Análise de imagem: Uma nova técnica para determinar a eficiência de panos de limpeza. Fibers Polym. Fiber Polym. 2006 , 7, 73–78. [ Google Scholar ] [ CrossRef ]
- Kandil, SM; Soliman, II; Diab, HM; Bedair, NI; Mahrous, MH; Abdou, EM Transportadores vesiculares de fosfato de ascorbil magnésio para administração tópica; preparação, avaliação in vitro e ex vivo, otimização fatorial e avaliação clínica em pacientes com melasma. Drug Deliv. 2022 , 29, 534–547. [ Google Scholar ] [ CrossRef ]
- Prendergast, PM Imagem da pele em medicina estética. Em Medicina estética: arte e técnicas; Prendergast, PM, Shiffman, MA, Eds.; Springer: Berlim/Heidelberg, Alemanha, 2012; pp. 59–68. ISBN 978-3-642-20113-4. [ Google Acadêmico ]
- Messaraa, C.; Metois, A.; Walsh, M.; Hurley, S.; Doyle, L.; Mansfield, A.; O'Connor, C.; Mavon, A. Medição de rugas e rugosidade pelo Antera 3D e sua aplicação para avaliação de produtos cosméticos. Skin Res. Technol. 2018 , 24, 359–366. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Francesco, A. Estudo clínico prospectivo randomizado de uma nova formulação tópica para redução de rugas faciais e regeneração dérmica. J. Cosmet. Dermatol. 2021 , 20, 2832–2840. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Anqi, S.; Xiukun, S.; Ai'e, X. Avaliação quantitativa de pele sensível por ANTERA 3D® combinado com GPSkin Barrier®. Skin Res. Technol. 2022 , 28, 840–845. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Parvar, SY; Amani, M.; Shafiei, M.; Rastaghi, F.; Hosseini, SA; Ahramiyanpour, N. A eficácia e os efeitos adversos das opções de tratamento para poros faciais: um artigo de revisão. J. Cosmet. Dermatol. 2023 , 22, 763–775. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- WaterWipe. Nossa história com lenços umedecidos para bebês|WaterWipes UK. WaterWipes. Disponível online: https://www.waterwipes.com/uk/en/our-story (acessado em 12 de julho de 2024).
- Marsh, RG; Miller, KH; Dannenberg, A. Método para avaliar a adesão de solos ou exsudatos à pele. US20100228107A1, 9 de setembro de 2010. Disponível online: https://patents.google.com/patent/US20100228107A1/en (acessado em 3 de julho de 2024).
- Jubinville, E.; Girard, M.; Trudel-Ferland, M.; Fliss, I.; Jean, J. Inativação do Norovírus Murino Suspenso em Matéria Orgânica Simulando Condições Reais de Contaminação Viral. Virol. 2021 , 13, 544–552. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Araco, F. Estudo preliminar prospectivo e randomizado de polinucleotídeo altamente purificado vs. placebo no tratamento de cicatrizes de acne moderadas a graves. Aesthet. Surg. J. 2021 , 41, NP866–NP874. [ Google Scholar ] [ CrossRef ]
- Niemeyer-van der Kolk, T.; Buters, TP; Krouwels, L.; Boltjes, J.; de Kam, ML; van der Wall, H.; van Alewijk, DCJG; van den Munckhof, EHA; Becker, MJ; Feiss, G.; et al. O peptídeo antimicrobiano tópico omiganan recupera a disbiose cutânea, mas não melhora os sintomas clínicos em pacientes com dermatite atópica leve a moderada em um ensaio clínico randomizado de fase 2. J. Am. Acad. Dermatol. 2022 , 86, 854–862. [ Google Scholar ] [ CrossRef ]
- Hossain, MM; Jones, JM; Dey, S.; Carr, GJ; Visscher, MO Quantificação da transferência de loção de lenços umedecidos para bebês para a pele de prematuros e neonatais. Food Chem. Toxicol. 2015 , 84, 106–114. [ Google Scholar ] [ CrossRef ]
- Gitlina, Y.; Guarnera, GC; Dhillon, DS; Hansen, J.; Lattas, A.; Pai, D.; Ghosh, A. Medição prática e reconstrução da reflectância espectral da pele. Comput. Graph. Fórum 2020 , 39, 75–89. [ Google Scholar ] [ CrossRef ]
- Messaraa, C.; Metois, A.; Walsh, M.; Flynn, J.; Doyle, L.; Robertson, N.; Mansfield, A.; O'Connor, C.; Mavon, A. Capacidades do Antera 3D para medições de poros. Skin Res. Technol. 2018 , 24, 606–613. [ Google Scholar ] [ CrossRef ]
- Vachiramon, V.; Namasondhi, A.; Anuntrangsee, T.; Kositkuljorn, C.; Jurairattanaporn, N. Um estudo de ultrassom microfocado combinado e preenchimento dérmico de ácido hialurônico no tratamento de poros faciais dilatados em asiáticos. J. Cosmet. Dermatol. 2021 , 20, 3467–3474. [ Google Scholar ] [ CrossRef ]
- Shahzad, Y.; Louw, R.; Gerber, M.; du Plessis, J. Rompendo a barreira da pele por meio de modulações de temperatura. J. Control. Release 2015 , 202, 1–13. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Johnson, JM; Kellogg, DL Controle térmico local da circulação cutânea humana. J. Appl. Physiol. 2010 , 109, 1229–1238. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Charkoudian, N. Fluxo sanguíneo da pele na termorregulação humana adulta: como funciona, quando não funciona e por quê. Mayo Clin. Proc. 2003 , 78, 603–612. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Park, H.-K.; Kim, S.-B. Atividade antimicrobiana do extrato de semente de toranja. Korean J. Food Nutr. 2006 , 19, 526–531. [ Google Scholar ]
- Sung-Hwan, CHO; Il-Won, SEO; Jong-Duck, C.; In-Saeng, JOO Atividade antimicrobiana e antioxidante do extrato de toranja e semente em produtos pesqueiros. Korean J. Fish. Aquat. Sci. 1990 , 23, 289–296. [ Google Scholar ]
- Jong-Duck, C.; Il-Won, SEO; Sung-Hwan, CHO Estudos sobre a atividade antimicrobiana do extrato de semente de toranja. Korean J. Fish. Aquat. Sci. 1990 , 23, 297–302. [ Google Scholar ]
- Saaty, AH Atividade antibacteriana e antiviral de extratos de sementes de toranja: Impacto anti-síndrome respiratória aguda grave do coronavírus 2. Arch. Pharm. Pract. 2022 , 13, 68–73. [ Google Scholar ] [ CrossRef ]
- Khaiat, A.; Saliou, C. Extratos botânicos. Em Cosmecêuticos e cosméticos ativos, 3ª ed.; CRC Press: Boca Raton, FL, EUA, 2015. [ Google Scholar ]
- Yarovaya, L.; Waranuch, N.; Wisuitiprot, W.; Khunkitti, W. Estudo clínico de alterações cutâneas asiáticas após aplicação de uma formulação de protetor solar contendo extrato de semente de uva. J. Cosmet. Dermatol. 2022 , 21, 4523–4535. [ Google Scholar ] [ CrossRef ]
- MTU. Política de Ética em Pesquisa Humana da MTU. Disponível online: https://www.mtu.ie/media/mtu-website/governance/policies-and-publications/academic-council-poli-cies-and-regulations/research-innovation-and-postgraduate-study/Human_Research_Ethics_Policy_AC_app_030622.pdf (acessado em 16 de julho de 2024).
- Wood, K. National Policy Statement on Ensuring Research Integrity in Ireland. Disponível online: https://www.iua.ie/publications/national-policy-statement-on-ensuring-research-integrity-in-ireland/ (acessado em 5 de setembro de 2024).
Aviso Legal/Nota do Editor: As declarações, opiniões e dados contidos em todas as publicações são exclusivamente dos autores e colaboradores individuais e não da MDPI e/ou do(s) editor(es). A MDPI e/ou o(s) editor(es) isentam-se de responsabilidade por quaisquer danos a pessoas ou propriedades resultantes de quaisquer ideias, métodos, instruções ou produtos mencionados no conteúdo.
© 2024 pelos autores. Licenciado MDPI, Basel, Suíça. Este artigo é um artigo de acesso aberto distribuído sob os termos e condições da licença Creative Commons Attribution (CC BY) ( https://creativecommons.org/licenses/by/4.0/ ).
More on the Skincare Hub
View allPele seca vs. pele desidratada: qual é a diferença e como cuidar dela?
Qual é a diferença e como cuidar dela?

Assaduras do Bebé
Assaduras são um problema comum que afeta muitos bebês, mas, para pais de primeira viagem, pode ser bastante angustiante ver seu pequeno desconfortável ou irritado. No entanto, existem algumas medidas que você pode tomar para ajudar a prevenir e controlar assaduras. Aqui, respondo a algumas das perguntas mais comuns sobre assaduras, e espero que ajudem você a cuidar do seu pequeno. – Dra. Alexis Granite