Seleziona Regione
-
Europe
-
Americas
-
Africa and Middle East
-
Asia Pacific
Arnold Marisa (1), Wisdom Shadrach (1), Kerrie Holohan (1), Abed Alkarem Abu Alhaija (2), Emer Gilligan (3), Jill Sommerville (3), Niall Burke (1) (*) e Tim Yeomans (1)
1 Centro di biotecnologia applicata Shannon, Munster Technological University, V92 CX88 Tralee, Irlanda; [email protected] (WS); [email protected] (TY)
2 Divisione di Bioscienze Orali, Dublin Dental Hospital, Trinity College Dublin, D02 F859 Dublino, Irlanda
3 WaterWipes UC., Donore Road Industrial Estate, Donore Road, Rathmullan, A92 VX00 Drogheda, Irlanda; [email protected] (EG); [email protected] (JS)
*Corrispondenza: [email protected]
Redattore accademico: Maria Manconi
Invio ricevuto: 31 luglio 2024 / Revisionato: 13 settembre 2024 / Accettato: 26 settembre 2024 / Pubblicato: 1 ottobre 2024
Astratto
Una funzionalità chiave delle salviette detergenti è la loro efficienza nel rimuovere lo sporco e la contaminazione microbica dalla pelle a livelli sicuri o non rilevabili, tradizionalmente determinati utilizzando il metodo gravimetrico, che è stato segnalato come soggetto a errori sperimentali. Questo studio valuta l'efficienza di una salvietta detergente a base d'acqua, WaterWipes® (WaterWipes, UC, Drogheda, Irlanda), per rimuovere materia fecale sintetica (Feclone™, SiliClone Creations LLC, Havertown, PA, Stati Uniti) ed Escherichia coli (NCTC 10538) dalla pelle dei volontari, la prima utilizzando un dispositivo di analisi dermica chiamato telecamera Antera 3D™ (Miravex Ltd., Dublino, Irlanda), e la seconda utilizzando metodi microbiologici standard. Feclone™ è stato applicato sugli avambracci dei partecipanti e la telecamera Antera 3D™ ha catturato immagini dettagliate della superficie della pelle prima e dopo la pulizia. L'approccio della telecamera Antera 3D™ si è rivelato efficace nel misurare l'efficienza della pulizia, con la pulizia che rimuove tutte le tracce rilevabili del Feclone™ applicato. L'area totale dei pori (mm2), il conteggio dei pori e il volume totale dei pori (mm3) nei partecipanti al test dopo la pulizia sono stati osservati ridotti in media rispettivamente del 39,05%, del 34,39% e del 39,98%. La pulizia ha rimosso il 99,99% di E. coli (NCTC 10538) applicato, come misurato utilizzando il metodo di conteggio delle piastre microbiche. In conclusione, si è osservato che il metodo della telecamera Antera 3D™ è efficace nel valutare la rimozione del Feclone™ applicato localmente.
Parole chiave: salviette detergenti; telecamera Antera 3D™; Feclone™; WaterWipes®; rimozione batterica
1. Introduzione
Le salviette possono essere descritte come agenti di pulizia e sono generalmente divise in salviette asciutte e umide, con l'uso di salviette umide in aumento negli ultimi anni, soprattutto in relazione all'igiene dei neonati e dei bambini [ 1 ]. Gli studi dimostrano che l'uso di salviette umide migliora i risultati della pulizia dei pannolini per bambini, offrendo una pulizia efficiente e un eritema cutaneo ridotto, adatto sia per superfici cutanee non danneggiate che danneggiate rispetto all'uso di acqua e stoffa [ 2 , 3 , 4 , 5 ]. Le salviette umide per bambini sono in genere costituite da materiali in fogli di base formulati con un tensioattivo detergente delicato, conservanti e agenti tampone del pH. L'acqua è generalmente utilizzata come componente di base nelle salviette per bambini allo scopo di pulire la pelle sensibile dei bambini e i residui fecali [ 4 , 6 ]. È stato raccomandato da una tavola rotonda europea che le salviette umide progettate principalmente per l'uso nei bambini non dovrebbero avere il potenziale di causare reazioni di sensibilità cutanea e dovrebbero essere formulate con ingredienti sicuri per un uso a lungo termine [ 7 ]. Le salviette umidificate progettate per applicazioni di pulizia e disinfezione vengono sottoposte a test standard, come test microbiologici, efficienza di pulizia, raccolta di salviette bagnate e formulazione della lozione [ 1 ], con l'efficienza di pulizia tradizionalmente determinata utilizzando metodi gravimetrici di pulizia (come la tecnica di recupero del cioccolato fuso) che sono stati segnalati come soggetti a errori sperimentali [ 1 , 8 ].
Pertanto, questo studio cerca di progettare e valutare un nuovo metodo non gravimetrico con potenziale utilizzo futuro per valutare l'efficienza di pulizia di prodotti di salviette commerciali nuovi ed esistenti. Il metodo progettato prevede l'uso di una telecamera Antera 3D™ nota per la sua imaging dermico in tempo reale, con vantaggi quali la fornitura di dati accurati, rapidi e oggettivi in diverse aree di studi sulla pelle e valutazione di prodotti cosmetici [ 9 , 10 , 11 , 12 ]. La telecamera Antera 3D™ (Miravex Ltd., Dublino, Irlanda), con brevetto europeo n. 2400890, funziona sul principio dell'illuminazione della pelle da più angolazioni, con dati sulla superficie della pelle riprodotti in modo 3D utilizzando software abilitato al computer per interpretare la luce riflessa dalla superficie della pelle. I dati cutanei rilevanti che possono essere generati con questo strumento includono conteggi dei pori della pelle, rughe, ruvidità e analisi della pigmentazione [ 13 ]. I pori della pelle svolgono un ruolo nel rilascio di sebo, sudore e detriti cellulari dalla pelle. È stato segnalato che il trattamento dei pori dilatati del viso (con terapie come ultrasuoni, luce a banda larga, radiofrequenza e laser frazionati non ablativi) è una delle principali richieste cosmetiche [ 14 ].
Il metodo progettato è stato valutato utilizzando WaterWipes® (WaterWipes UC, Drogheda, Irlanda), un marchio disponibile in commercio di salviette umidificate senza tensioattivi realizzate con ingredienti minimi. La sua composizione di base comprende materiali fibrosi privi di plastica (fogli inumiditi di tessuto non tessuto spun lace 100% viscosa). I fogli sono inumiditi con acqua ultrapurificata (99,9%) ed estratto di semi di citrus grandis (pompelmo) 0,1% [ 15 ]. La sua efficacia pulente è stata testata contro applicazioni topiche di FecloneTM ed E. coli in due distinti studi su volontari umani. FecloneTM (SiliClone Creations LLC, Havertown, PA, Stati Uniti) è un marchio proprietario di materiale fecale simulato artificiale con applicazioni segnalate nei test di prodotti alimentari nonché salviette per l'incontinenza e per neonati [ 16 , 17 ]. È stato utilizzato il metodo adattato della telecamera Antera 3DTM per valutare l'efficacia della pulizia di uno specifico prodotto per salviette disponibile in commercio nella sperimentazione FecloneTM e il metodo di conteggio delle piastre per la sperimentazione sull'E. coli.
2. Materiali e metodi
2.1. Valutazione dell'efficacia della pulizia con prodotti Wipe nella rimozione di Feclone™
Questo studio è stato condotto sulla base dell'approvazione etica del Comitato etico per la ricerca umana della Munster Technological University (HREC-FER-24-004) e ha funzionato in linea con BS EN 1500:2013 [ 1 ]. I criteri di inclusione per lo studio erano maschi e femmine di età superiore ai 18 anni con pelle umana adulta sana, intatta e non sensibile, mentre i criteri di esclusione erano adulti vulnerabili, disturbi della pelle, sensibilità cutanea (auto-riportata) o pelle rotta sull'avambraccio. Il pannello risultante era composto da 25 volontari umani (18 femmine e 7 maschi) volontari; i campioni e le immagini scattate sono stati resi anonimi ai partecipanti. La fascia di età dei partecipanti a questo studio era 18-50. L'indagine è stata condotta in un ambiente controllato presso lo Shannon Applied Biotechnology Centre Laboratory (MTU, Kerry, Irlanda) con temperatura ambiente (25 ± 2 °C) e umidità relativa (50 ± 5%).
2.1.1. Preparazione di Feclone™
In totale, 120 mL di acqua distillata sono stati riscaldati a 99 °C in un recipiente coperto; contemporaneamente, 40 g di Feclone™ sono stati preriscaldati per 5 minuti utilizzando una piastra riscaldante. Una volta raggiunta la temperatura desiderata, l'acqua riscaldata è stata aggiunta con attenzione al Feclone™ (SiliClone Creations LLC, Havertown, PA, USA), seguita da un'agitazione accurata per circa 20 s utilizzando una spatola. La miscela è stata quindi coperta con un foglio di alluminio e incubata a 99 °C per un minimo di 30 minuti, con la miscela delicatamente agitata dopo i primi 10 minuti. Alla fine del periodo di incubazione, è stata eseguita un'ultima breve agitazione prima di aliquotare la soluzione calda in provette da 50 mL. Le provette sono state poste a 4 °C fino a ulteriore utilizzo.
2.1.2. Applicazione di Feclone™ sull'avambraccio umano
I volontari si sono seduti con un braccio appoggiato a un tavolo e con l'avambraccio esposto e hanno lasciato che si acclimatassero alle condizioni della stanza per 3 minuti. Lo scopo di questo studio era determinare l'efficacia della pulizia della salvietta, quindi la temperatura della pelle è stata considerata una priorità inferiore. All'interno di una sezione di 8 × 8 cm, un'area di 4 × 4 cm è stata assicurata posizionando un modello sull'avambraccio del volontario. Una quantità di 2 g di Feclone™ è stata applicata all'area di 4 × 4 cm e distribuita uniformemente utilizzando una spatola. La procedura di pulizia ha comportato la pulizia dell'area contaminata in verticale e in orizzontale come segue: da sinistra a destra con una superficie di pulizia, seguita da destra a sinistra con un'altra superficie di pulizia, quindi dall'alto verso il basso con una nuova superficie di pulizia e infine dal basso verso l'alto utilizzando una nuova superficie di pulizia, tutto dallo stesso foglio.
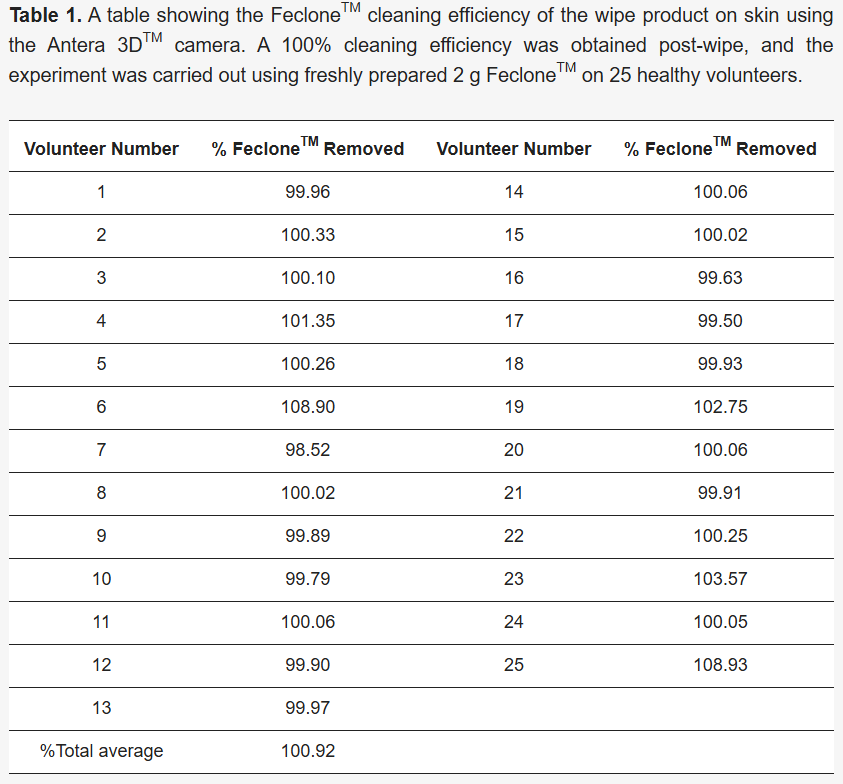
Un'immagine dell'area contrassegnata è stata catturata utilizzando una telecamera Antera 3D™ prima e dopo la pulizia, nonché direttamente dopo l'applicazione di Feclone™, e analizzata utilizzando il software Antera 3D™ (versione 3.1.8) per confrontare le condizioni pre-pulizia e post-pulizia. La percentuale di rimozione è stata calcolata utilizzando il parametro del volume del software, che misura la depressione e l'elevazione su una superficie di riferimento normalizzata. Il volume della pelle (mm3) post-pulizia è stato sottratto dal volume della pelle pre-applicazione di FecloneTM; il valore ottenuto è stato sottratto dal volume della pelle (mm3) con Feclone™ pre-pulizia e diviso per il volume della pelle (mm3) con Feclone™ pre-pulizia. Questo valore è stato quindi moltiplicato per 100 per calcolare la percentuale di rimozione (formula nella Sezione 3.1 ) con il risultato ottenuto trovato nella Sezione 3.1 ( Tabella 1 ).
2.2. Valutazione dell'impatto del prodotto di pulizia sui pori della pelle umana
Questo studio è stato condotto sull'avambraccio nudo di ogni volontario (25 in totale). L'area di prova è stata contrassegnata sul braccio come descritto in precedenza in modo che le immagini prima e dopo fossero esattamente della stessa area. L'area è stata quindi fotografata, seguita da un'applicazione di 2 g di Feclone™. La successiva procedura di pulizia è stata condotta come descritto nella Sezione 2.1.2 e i risultati ottenuti possono essere trovati nella Sezione 3.2 ( Tabella 2 ). La formula utilizzata per i diversi parametri dei pori dal software Antera 3D™ (versione 3.1.8) include:
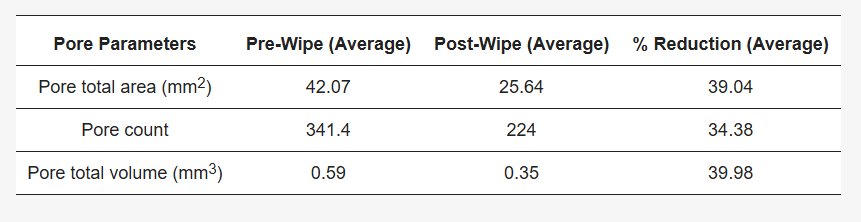
Tabella 2. Una tabella che mostra l'impatto della salvietta di prova sui pori della pelle. I dati sono stati ottenuti e analizzati utilizzando il metodo della telecamera Antera 3D™. È stata osservata una significativa riduzione del conteggio medio dei pori, del volume e dell'area dopo la salvietta rispetto all'imaging pre-salviette della stessa superficie cutanea.
- Volume totale dei pori (mm3) V = somma della profondità per ogni pixel * area del pixel.
- Area totale dei pori (mm2) = numero di pixel depressi * area dei pixel.
- Conteggio dei pori = isole di depressione isolate all'interno della regione di interesse selezionata.
2.3. Valutazione dell'efficacia della pulizia dei prodotti Wipe contro l'Escherichia coli (NCTC 10538)
Questo studio è stato condotto utilizzando KWIK STIK E. coli (NCTC 10538), terreni di coltura batterica e 25 volontari umani. La preparazione dei terreni di coltura e delle colture batteriche starter è stata preparata prima del test sui volontari.
2.3.1. Coltura batterica
In totale, 30 g di Tryptone soya broth (TSB) in polvere sono stati aggiunti a 100 mL di acqua distillata. La miscela è stata mescolata accuratamente fino a quando la polvere non si è completamente sciolta. Il volume è stato quindi regolato con acqua distillata per ottenere un volume finale di 1 L. Successivamente, il terreno è stato sterilizzato in autoclave. Il terreno Tryptone soya agar (TSA) è stato preparato in modo simile, ma utilizzando 40 g/L di polvere di TSA.
Le cellule di Escherichia coli (E. coli) (NCTC 10538) sono state inizialmente inoculate su piastre TSA e poi poste in un'incubatrice impostata a 37 °C durante la notte. Il giorno seguente, è stata selezionata una singola colonia e trasferita su un'altra piastra TSA, che è stata poi incubata nelle stesse condizioni. Il giorno seguente, è stata prelevata una singola colonia e introdotta in 10 mL di terreno TSB. Questa coltura è stata incubata durante la notte a temperatura ambiente con agitazione. Il giorno dopo, la densità ottica (DO) della coltura è stata misurata utilizzando uno spettrofotometro e le cellule sono state diluite con terreno TSB fino a raggiungere una DO di 0,15.
2.3.2. Applicazione di batteri all'avambraccio dei volontari
Questo metodo si basava sulle linee guida delineate in BS EN 1500:2013 [ 1 ]. Le colture di brodo di E. coli con una densità ottica (DO) di 0,15 sono state utilizzate costantemente durante l'esperimento; il numero medio di E. coli utilizzato era 1,55 × 108 CFU/mL. Un'aliquota di questa coltura è stata utilizzata per l'enumerazione utilizzando il metodo di conteggio delle piastre. I volontari hanno pulito le loro mani e braccia con un sapone non antibatterico, seguito dal tampone dell'area pulita, che è stata posta in 1 mL di terreno di coltura salina tamponata con fosfato (PBS) per l'enumerazione tramite il metodo di conteggio delle piastre (che fungeva da controllo). Un'area di 4 × 4 cm è stata contrassegnata sulla pelle del volontario per il test. Successivamente, 100 µL di coltura notturna a DO di 0,15 sono stati pipettati sull'area di prova, distribuiti delicatamente utilizzando uno spanditore a forma di L e lasciati asciugare all'aria per 3 minuti.
Questa è stata seguita dalla procedura di pulizia utilizzando il prodotto per salviette come descritto nella Sezione 2.1.2 . La salvietta usata è stata quindi immersa in 10 mL di terreno di coltura neutralizzante Dey-Engley (D3435, Merck, Darmstadt, Germania), agitata per 60 s e diluita in serie due volte con terreno PBS. Successivamente, 0,1 mL dei batteri sono stati applicati a una piastra di agar per la coltura notturna e la successiva quantificazione. Dopo il processo di pulizia, la superficie dell'area di prova dell'avambraccio è stata tamponata con un tampone inumidito. Il tampone è stato quindi inserito in 1 mL di terreno PBS e 0,1 mL sono stati applicati a una piastra di agar per la quantificazione. Diluizioni seriali di puro, 10−1 e 10−2 sono state applicate a una piastra di agar per la quantificazione in triplicato. Lo stock originale di batteri è stato diluito in serie a 10−3, 10−4 e 10−5 e piastrato su piastre di agar per la conta delle colonie. Per ciascuna area, è stato calcolato CFU/mL utilizzando la seguente formula:
CFU/mL=(N ∗ DF)/VCCFU/mL=(N ∗ DF)/VC
dove CFU/mL = Unità formanti colonie per mL:
N = Numero di colonie (numero totale di colonie contate sulle piastre entro l'intervallo ottimale).
DF = Fattore di diluizione (il reciproco della diluizione utilizzata per la placcatura).
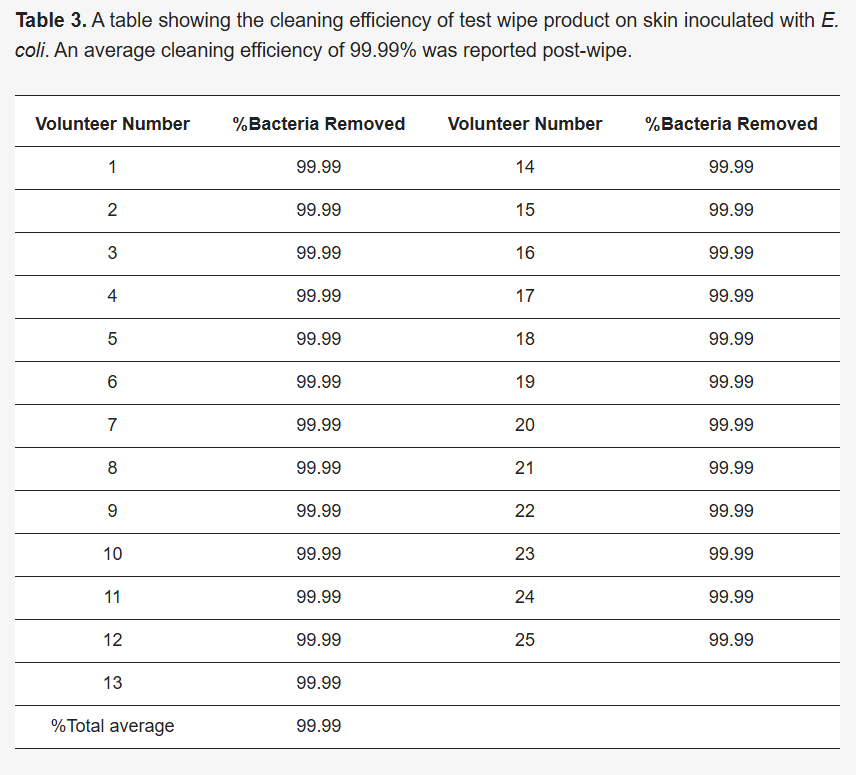
VC = Volume di coltura piastrata (il volume della coltura diluita piastrata sulla piastra di agar). La tabella che mostra la percentuale di batteri rimossi può essere trovata nella Sezione 3.3 ( Tabella 3 ).
3. Risultati
3.1. Valutazione dell'efficienza di pulizia del prodotto Wipe nella rimozione del materiale fecale simulato (Feclone™)
Il metodo Antera 3D™ adattato è stato utilizzato per valutare l'efficacia della pulizia delle salviette di prova relativamente alla rimozione di Feclone™ dagli avambracci dei volontari. I risultati sono stati analizzati utilizzando il parametro volume del software Antera 3D™. Il volume si riferisce allo spessore o alla voluminosità complessiva di qualsiasi residuo o contaminante sulla superficie della pelle e la riduzione del volume dopo la pulizia indica una rimozione riuscita (vedere Figura 1 ). La percentuale di rimozione è stata calcolata utilizzando la seguente formula:
𝑠𝑣0−𝑠𝑣1⁄𝑠𝑣0×100sv0−sv1∕sv0×100
dove SV0 = Volume della pelle (mm3) con pre-pulizia con Feclone™.
SV1 = (Volume della pelle (mm3) dopo la pulizia—volume della pelle (mm3) prima dell'applicazione di Feclone™).
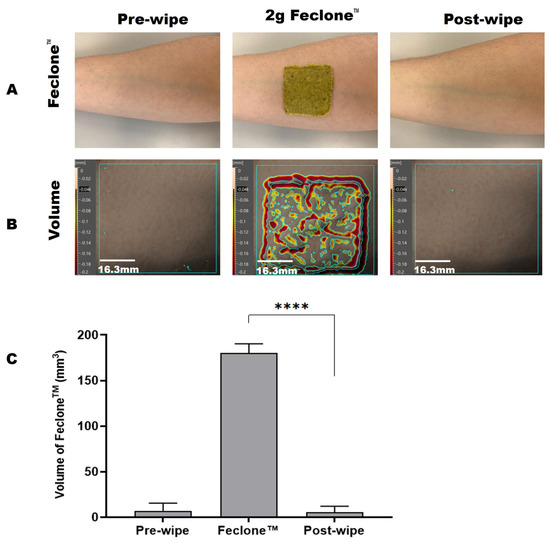
Figura 1. ( A ) Immagini rappresentative che mostrano la pelle umana dell'avambraccio prima e dopo l'applicazione e la rimozione di Feclone™ utilizzando il prodotto di prova; l'immagine è stata eseguita utilizzando una fotocamera del telefono. ( B ) Volume di Feclone™ rilevato sulla superficie cutanea dell'avambraccio utilizzando il metodo Antera 3D™ e la pulizia con il prodotto di prova. L'area di applicazione per l'analisi era di 40 mm × 40 mm. La barra della scala verticale rappresenta il volume e la topografia della pelle, mentre la barra della scala orizzontale si riferisce alla misurazione 2D della regione cutanea definita. ( C ) Mostra i volumi cutanei pre-pulizia, Feclone™ e post-pulizia osservati con il metodo Antera 3DTM. È stato notato che il prodotto di prova riduceva l'aumento del volume cutaneo indotto da Feclone™ fino ai livelli pre-applicazione. Un'analisi t-test accoppiata del volume cutaneo residuo somministrato con Feclone™ e post-pulizia ha mostrato una differenza altamente significativa (**** p < 0,0001). Il grafico è stato tracciato come media con SD (deviazione standard) utilizzando GraphPad Prism 10 (GraphPad Software, 225 Franklin Street, Fl. 26 Boston, MA 02110, USA). Ciò rappresenta un'efficienza di pulizia media del 100,92%.
3.2. Valutazione del prodotto di pulizia sui pori della pelle umana
Dopo aver pulito la pelle dell'avambraccio del volontario con il prodotto per la pulizia, è stata osservata una riduzione nei parametri dei pori, quali il numero totale dei pori, il volume dei pori e l'area ( Figura 2 ).
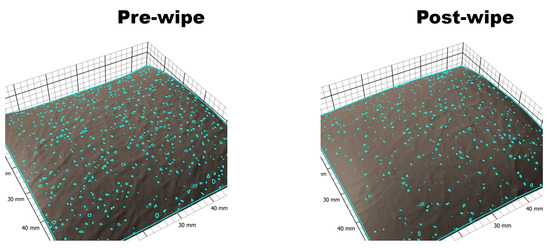
Figura 2. Un'immagine rappresentativa del software Antera 3DTM che mostra la riduzione osservata nei pori cutanei rilevabili (conteggio, area totale, volume totale) dopo la pulizia con il prodotto per la pulizia.
3.3. Valutazione dell'efficacia della pulizia con prodotti per la pulizia nella rimozione dell'Escherichia coli
È stata valutata anche l'efficacia del prodotto di pulizia nella rimozione della contaminazione batterica. È stato calcolato il numero di CFU/mL per ciascuna area e sono state determinate le medie. Questi risultati indicano che il prodotto di pulizia ha rimosso efficacemente il 99,99% delle cellule batteriche e ha pulito in modo efficiente le aree cutanee contaminate. Ciò è stato convalidato raccogliendo le salviette usate per la quantificazione batterica dopo la pulizia, nonché tamponando l'area pulita per la coltura su piastre TSA (vedere Figura 3 A,B).
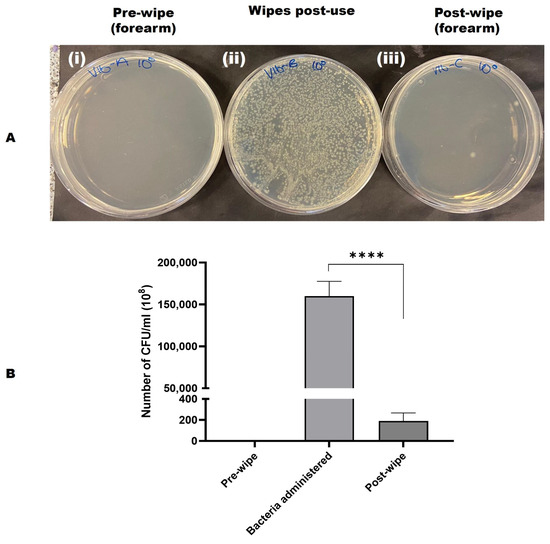
Figura 3. ( A ) Un'immagine rappresentativa che mostra l'efficienza di rimozione batterica delle salviette di prova dalla pelle umana contaminata. ( i ) Tampone pre-pulizia piastrato ( ii ) Salvietta usata piastrato ( iii ) Tampone post-pulizia piastrato. V = volontario, A = Campione pre-pulizia, B = Salvietta post-uso, C = Campione post-pulizia, 100 = campione puro/non diluito. ( B ) Grafico dell'efficienza di rimozione batterica del prodotto per salviette utilizzando E. coli e conteggio microbiologico. È stato osservato che le salviette di prova hanno rimosso il 99,99% dei batteri di ciò che è stato somministrato. L'analisi del t-test accoppiato dei batteri somministrati e il conteggio post-pulizia hanno mostrato una differenza altamente significativa (**** p < 0,0001). Il grafico è stato tracciato come media con SD (deviazione standard) utilizzando GraphPad Prism 10. V = volontario, A = campione pre-pulizia, B = pulizia post-uso, C = campione post-pulizia, 100 = campione puro/non diluito.
4. Discussion
Questo studio mirava a progettare e valutare un metodo alternativo per condurre studi sull'efficienza di pulizia dei prodotti per salviette utilizzando una telecamera Antera 3D™, un dispositivo di imaging e analisi dermica. In questo studio sono state utilizzate salviette per neonati disponibili in commercio (WaterWipes®) e sono state testate per la loro efficienza di pulizia con materia fecale sintetica (Feclone™) ed E. coli contaminante dalla superficie cutanea degli avambracci dei volontari. La telecamera Antera 3D™, uno strumento di valutazione dei prodotti cosmetici convalidato [ 11 ], è stata impiegata in molti studi cosmetici come quelli che coinvolgono la quantificazione di rughe, acne e pigmentazione [ 11 , 18 , 19 ], e quindi è stato sviluppato e testato un adattamento dello standard europeo BS EN 1500:2013 [ 1 ] che incorpora la telecamera Antera 3D™ per la valutazione quantitativa e qualitativa dell'efficienza di pulizia delle salviette utilizzando il prodotto per salviette. L'analisi oggettiva del test FecloneTM ha utilizzato il parametro del volume del software per fornire una valutazione approfondita dell'efficienza di pulizia delle salviette.
I risultati della valutazione visiva e dell'analisi della telecamera Antera 3D™ hanno dimostrato che questo metodo era appropriato per valutare la rimozione di Feclone™ dalla pelle umana utilizzando salviette, che hanno mostrato un'efficienza di pulizia Feclone™ del 100,92%. Ipotizziamo che il valore di rimozione >100% potrebbe essere dovuto alla sensibilità del metodo della telecamera Antera 3D™ nel rilevare la rimozione tramite salvietta sia di Feclone™ applicato che di eventuali detriti cutanei preesistenti. Un approccio di imaging simile per determinare l'efficienza di pulizia tramite salviette è stato riportato da Lee et al. [ 8 ] e consiste in un computer con uno scanner e un software di analisi delle immagini; tuttavia, questo studio è stato condotto utilizzando un contaminante distribuito su una lastra di vetro e non sulla pelle umana. Le tecniche di imaging forniscono quindi un'alternativa al tradizionale metodo gravimetrico utilizzato per valutare l'efficienza di pulizia delle salviette, che è stato segnalato come soggetto a errori sperimentali.
Il metodo gravimetrico in genere prevede la registrazione del peso della salvietta prima e dopo la pulizia per determinare l'efficienza della pulizia. Questa tecnica si concentra sull'analisi della salvietta e non della superficie da pulire. È stato segnalato che il metodo è soggetto a errori che potrebbero derivare dal processo, come dalla manipolazione delle salviette durante il processo di pesatura che potrebbe portare al trasferimento di umidità dalla salvietta ai guanti del tester e all'inevitabile evaporazione dell'umidità dalle salviette di prova, tutti fattori che potrebbero influenzare i risultati ottenuti e dovrebbero essere considerati come variabili sperimentali. Tuttavia, con il metodo della telecamera Antera 3D™, che è un approccio basato sull'ottica, c'è meno preoccupazione per l'evaporazione dell'umidità della salvietta e la manipolazione, poiché l'efficienza della pulizia verrà dedotta direttamente dalla superficie della pelle e non tramite la differenza nei pesi delle salviette, rendendo questo metodo potenzialmente utile per affrontare gli errori comuni all'analisi gravimetrica. Altri vantaggi associati ai metodi proposti con la telecamera Antera 3D™ includono la sua capacità di imaging cutaneo 3D, facilità d'uso, precisione, riproducibilità e la sua lettura multipla per parametri cutanei quali dimensioni dei pori, imperfezioni, rughe e ruvidità. Tuttavia, sono state osservate alcune limitazioni con i modelli proposti, che includono l'incertezza sulla sua applicabilità in altre aree di caratterizzazione dell'efficienza delle salviette umidificate quali l'analisi della velocità di asciugatura delle salviette (velocità di evaporazione dell'umidità dalle salviette quando esposte all'atmosfera nel tempo), l'analisi del prelievo delle salviette (capacità del bagnato di raccogliere la lozione) e gli studi sul trasferimento della lozione (rilascio della lozione dalle salviette alla pelle) [ 1 , 8 , 20 ]. Poiché il metodo proposto utilizza un dispositivo specifico, la telecamera Antera 3D™ e il software associato sono necessari per eseguire o riprodurre il metodo, una potenziale limitazione di applicazione diffusa. Il modello è una tecnica ottica con variabili quali distanza fissa, grado di risoluzione (0,1 mm) e banda spettrale (sette) ottenibili con la telecamera Antera 3D™, rendendo la topografia cutanea ricostruita una stima [ 21 ]. La sensibilità della tecnica proposta consente di rilevare ciò che è presente sulla pelle (peli, pori, sebo, cicatrici, lentiggini, ecc.); tuttavia, non ci si aspetta che ciò influenzi o causi artefatti nei dati generati, poiché il protocollo afferma che le letture di base della pelle devono essere prese prima.
È interessante notare che è stato osservato che la pulizia della pelle con il prodotto di salvietta in questione ha avuto un impatto sulla riduzione del numero totale di pori medi, del volume e dell'area, e questo è di notevole importanza, poiché vari studi hanno dimostrato una relazione tra un numero inferiore di pori e una pelle più sana [ 14 , 22 , 23 ]. Ciò è probabilmente attribuito alla combinazione della formulazione e della composizione della salvietta, per cui una formulazione a bassa tensione superficiale si diffonde e bagna i pori della pelle in modo sufficiente da consentire alla salvietta di pulire efficacemente i pori da sebo, sudore e altri detriti cellulari. La riduzione del numero medio di pori e delle dimensioni può anche essere favorita dalla temperatura più fredda delle salviette stesse. La temperatura delle salviette sembra più fredda della temperatura della pelle; pertanto, questo potrebbe essere il motivo per cui i pori si chiudono temporaneamente. Alcuni studi hanno riportato che il raffreddamento della pelle porta a una riduzione delle dimensioni e del numero di pori tramite vasocostrizione cutanea e rassodamento della pelle [ 24 , 25 , 26 ]. Inoltre, l'estratto di semi di pompelmo (GSE), un ingrediente condizionante per la pelle e un ingrediente nel prodotto per salviette utilizzato, è stato segnalato per avere proprietà antimicrobiche [ 27 , 28 , 29 , 30 ]. È stato anche segnalato che possiede attività antiossidante e aiuta ad alleviare la congestione della pelle purificando, pulendo e liberando i pori ostruiti per una pelle liscia e luminosa, oltre a restringere i pori della pelle grazie alla sua capacità opacizzante [ 31 , 32 ]. Si propone che queste salviette, WaterWipes® (WaterWipes UC, Drogheda, Irlanda), potrebbero trovare impiego come un modo meno invasivo per pulire i pori e minimizzarne l'aspetto, dato che, se prese nel loro insieme, il cambiamento nell'area, nel volume e nel conteggio dei pori dopo la salvietta potrebbe essere una combinazione di tutti i motivi sopra menzionati; tuttavia, questo è un argomento separato e sono necessarie ulteriori ricerche per convalidare questi risultati e determinare l'esatto meccanismo d'azione, poiché le temperature delle salviette e della pelle dei volontari non sono state prese in considerazione in questo studio. Tuttavia, le capacità di visualizzazione e misurazione dei pori della telecamera Antera 3D™ (Miravex Ltd., Dublino, Irlanda) hanno fornito un'ulteriore comprensione dell'effetto che il prodotto per salviette ha sulla pelle.
5. Conclusioni
In conclusione, i risultati di questo studio dimostrano che il metodo della telecamera Antera 3D™ può essere una tecnica alternativa efficace per valutare l'efficienza delle salviette detergenti. I suoi vantaggi includono la semplicità d'uso, la riproducibilità dei dati, la luce controllata nell'area dell'immagine interna e il fatto che si tratti di un'unità portatile con un'alta risoluzione e una lettura multiparametrica. Tuttavia, poiché non è stato effettuato alcun confronto con altri metodi di valutazione dell'efficienza di pulizia (come la tecnica gravimetrica), questa tecnica proposta intende fungere da potenziale alternativa ai metodi esistenti. Il prodotto per salviette utilizzato in questo studio ha dimostrato di avere una buona efficienza di pulizia per quanto riguarda la rimozione sostanziale sia di Feclone™ che di E. coli dalla pelle umana. Ulteriori ricerche potrebbero esplorare le prestazioni delle salviette su diversi tipi di pelle e parti del corpo e in diverse condizioni ambientali per ampliare la loro applicabilità e comprensione dell'efficienza utilizzando il metodo sviluppato. Nel complesso, questo studio fornisce preziose informazioni sull'efficacia del metodo della telecamera Antera 3D™ per misurare l'efficienza di pulizia delle salviette detergenti.
Contributi dell'autore
Concettualizzazione, TY, NB, JS e EG; metodologia, AAAA, AM; KH e NB; indagine e analisi dei dati, AM, KH e WS; stesura: preparazione della bozza originale, WS; stesura: revisione e modifica, WS, NB, JS, EG e TY; risorse, EG, JS e TY; supervisione, NB e TY; amministrazione e finanziamento del progetto, TY, EG e JS Tutti gli autori hanno letto e accettato la versione pubblicata del manoscritto.
Finanziamento
Questa ricerca ha ricevuto finanziamenti da WaterWipes UC.
Dichiarazione del comitato di revisione istituzionale
Questo studio su volontari umani è stato condotto in conformità con la Dichiarazione di Helsinki e approvato dal Comitato etico per la ricerca umana della Munster Technological University (riferimento MTU-HREC-FER-24-004). La governance del Comitato etico per la ricerca umana della Munster Technological University è come delineato nella Politica etica per la ricerca umana dell'Università [ 33 ], ed è in linea con la Dichiarazione politica nazionale per garantire l'integrità della ricerca in Irlanda (Research Integrity National Forum (2019) [ 34 ]. Tutte le attività di ricerca che coinvolgono esseri umani come partecipanti alla ricerca devono essere sottoposte a revisione etica formale, prima dell'inizio.
Dichiarazione di consenso informato
Tutti i volontari hanno fornito il consenso informato scritto prima di partecipare a questo studio.
Dichiarazione di disponibilità dei dati
Tutti i dati sono reperibili in questo articolo.
Ringraziamenti
A tutti i volontari di entrambi gli studi viene riconosciuto il ruolo svolto nella raccolta dei dati.
Conflitti di interessi
Gli autori Jill Sommerville ed Emer Gilligan erano impiegati presso la società WaterWipes UC. Gli autori rimanenti dichiarano che la ricerca è stata condotta in assenza di relazioni commerciali o finanziarie che potrebbero essere interpretate come un potenziale conflitto di interessi.
Riferimenti
- Cheriaa, R.; Boubaker, J. Valutazione della qualità delle salviette umidificate per bambini. J. Ind. Text. 2022 , 51, 2124S–2147S. [ Google Scholar ] [ CrossRef ]
- Visscher, M.; Odio, M.; Taylor, T.; White, T.; Sargent, S.; Sluder, L.; Smith, L.; Flower, T.; Mason, B.; Rider, M.; et al. Cura della pelle nel paziente della TIN: effetti delle salviette rispetto a panno e acqua sull'integrità dello strato corneo. Neonatology 2009 , 96, 226–234. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Garcia Bartels, N.; Massoudy, L.; Scheufele, R.; Dietz, E.; Proquitté, H.; Wauer, R.; Bertin, C.; Serrano, J.; Blume-Peytavi, U. Regime standardizzato di cura del pannolino: uno studio pilota prospettico e randomizzato sulla funzione di barriera cutanea e IL-1α epidermica nei neonati. Pediatr. Dermatol. 2012 , 29, 270–276. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Rodriguez, KJ; Cunningham, C.; Foxenberg, R.; Hoffman, D.; Vongsa, R. La scienza alla base delle salviette umidificate per la pelle dei neonati: revisione degli ingredienti, sicurezza ed efficacia. Pediatr. Dermatol. 2020 , 37, 447–454. [ Google Scholar ] [ CrossRef ]
- Odio, M.; Streicher-Scott, J.; Hansen, RC Salviette monouso per neonati: efficacia e delicatezza sulla pelle. Dermatol. Nurs. 2001 , 13, 107–112, 117–118, 121. [ Google Scholar ]
- Ehretsmann, C.; Schaefer, P.; Adam, R. Tolleranza cutanea delle salviette umidificate per neonati da parte di neonati con dermatite atopica e confronto della delicatezza delle salviette umidificate per neonati e dell'acqua sulla pelle dei neonati. J. Eur. Acad. Dermatol. Venereol. 2001 , 15, 16–21. [ Google Scholar ] [ CrossRef ]
- Blume-Peytavi, U.; Lavender, T.; Jenerowicz, D.; Ryumina, I.; Stalder, J.; Torrelo, A.; Cork, MJ Raccomandazioni da una tavola rotonda europea sulle migliori pratiche per una sana cura della pelle dei neonati. Pediatr. Dermatol. 2016 , 33, 311–321. [ Google Scholar ] [ CrossRef ]
- Lee, J.; Kim, S.; Oh, KW Analisi delle immagini: una nuova tecnica per determinare l'efficienza dei panni per la pulizia. Fibre Polym. Fibre Polym. 2006 , 7, 73–78. [ Google Scholar ] [ CrossRef ]
- Kandil, SM; Soliman, II; Diab, HM; Bedair, NI; Mahrous, MH; Abdou, EM Trasportatori vescicolari di ascorbil fosfato di magnesio per somministrazione topica; preparazione, valutazione in vitro ed ex vivo, ottimizzazione fattoriale e valutazione clinica in pazienti con melasma. Drug Deliv. 2022 , 29, 534–547. [ Google Scholar ] [ CrossRef ]
- Prendergast, PM Skin Imaging in Medicina Estetica. In Medicina Estetica: Arte e Tecniche; Prendergast, PM, Shiffman, MA, Eds.; Springer: Berlino/Heidelberg, Germania, 2012; pp. 59–68. ISBN 978-3-642-20113-4. [ Google Scholar ]
- Messaraa, C.; Metois, A.; Walsh, M.; Hurley, S.; Doyle, L.; Mansfield, A.; O'Connor, C.; Mavon, A. Misurazione delle rughe e della rugosità mediante Antera 3D e sua applicazione per la valutazione dei prodotti cosmetici. Skin Res. Technol. 2018 , 24, 359–366. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Francesco, A. Studio clinico randomizzato prospettico di una nuova formulazione topica per la riduzione delle rughe del viso e la rigenerazione dermica. J. Cosmet. Dermatol. 2021 , 20, 2832–2840. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Anqi, S.; Xiukun, S.; Ai'e, X. Valutazione quantitativa della pelle sensibile mediante ANTERA 3D® combinato con GPSkin Barrier®. Skin Res. Technol. 2022 , 28, 840–845. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Parvar, SY; Amani, M.; Shafiei, M.; Rastaghi, F.; Hosseini, SA; Ahramiyanpour, N. L'efficacia e gli effetti avversi delle opzioni di trattamento per i pori del viso: un articolo di revisione. J. Cosmet. Dermatol. 2023 , 22, 763–775. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- WaterWipe. La nostra storia sulle salviette per bambini|WaterWipes UK. WaterWipes. Disponibile online: https://www.waterwipes.com/uk/en/our-story (accesso 12 luglio 2024).
- Marsh, RG; Miller, KH; Dannenberg, A. Metodo per valutare l'adesione di terreni o essudati alla pelle. US20100228107A1, 9 settembre 2010. Disponibile online: https://patents.google.com/patent/US20100228107A1/en (consultato il 3 luglio 2024).
- Jubinville, E.; Girard, M.; Trudel-Ferland, M.; Fliss, I.; Jean, J. Inattivazione del norovirus murino sospeso in materia organica che simula le condizioni reali di contaminazione virale. Food Environ. Virol. 2021 , 13, 544–552. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Araco, F. Studio preliminare prospettico e randomizzato di polinucleotide altamente purificato rispetto al placebo nel trattamento di cicatrici da acne da moderate a gravi. Aesthet. Surg. J. 2021 , 41, NP866–NP874. [ Google Scholar ] [ CrossRef ]
- Niemeyer-van der Kolk, T.; Buters, TP; Krouwels, L.; Boltjes, J.; de Kam, ML; van der Wall, H.; van Alewijk, DCJG; van den Munckhof, EHA; Becker, MJ; Feiss, G.; et al. Il peptide antimicrobico topico omiganan recupera la disbiosi cutanea ma non migliora i sintomi clinici nei pazienti con dermatite atopica da lieve a moderata in uno studio randomizzato controllato di fase 2. J. Am. Acad. Dermatol. 2022 , 86, 854–862. [ Google Scholar ] [ CrossRef ]
- Hossain, MM; Jones, JM; Dey, S.; Carr, GJ; Visscher, MO Quantificazione del trasferimento di lozione per salviette umidificate per neonati sulla pelle di neonati prematuri e neonatali. Food Chem. Toxicol. 2015 , 84, 106–114. [ Google Scholar ] [ CrossRef ]
- Gitlina, Y.; Guarnera, GC; Dhillon, DS; Hansen, J.; Lattas, A.; Pai, D.; Ghosh, A. Misurazione pratica e ricostruzione della riflettanza spettrale della pelle. Grafico di calcolo. Forum 2020 , 39, 75–89. [ Google Scholar ] [ CrossRef ]
- Messaraa, C.; Metois, A.; Walsh, M.; Flynn, J.; Doyle, L.; Robertson, N.; Mansfield, A.; O'Connor, C.; Mavon, A. Funzionalità Antera 3D per le misurazioni dei pori. Skin Res. Technol. 2018 , 24, 606–613. [ Google Scholar ] [ CrossRef ]
- Vachiramon, V.; Namasondhi, A.; Anuntrangsee, T.; Kositkuljorn, C.; Jurairattanaporn, N. Uno studio combinato di ultrasuoni microfocalizzati e filler dermico all'acido ialuronico nel trattamento dei pori facciali dilatati negli asiatici. J. Cosmet. Dermatol. 2021 , 20, 3467–3474. [ Google Scholar ] [ CrossRef ]
- Shahzad, Y.; Louw, R.; Gerber, M.; du Plessis, J. Violazione della barriera cutanea attraverso modulazioni della temperatura. J. Control. Release 2015 , 202, 1–13. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Johnson, JM; Kellogg, DL Controllo termico locale della circolazione cutanea umana. J. Appl. Physiol. 2010 , 109, 1229–1238. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Charkoudian, N. Flusso sanguigno cutaneo nella termoregolazione umana adulta: come funziona, quando non funziona e perché. Mayo Clin. Proc. 2003 , 78, 603–612. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Park, H.-K.; Kim, S.-B. Attività antimicrobica dell'estratto di semi di pompelmo. Korean J. Food Nutr. 2006 , 19, 526–531. [ Google Scholar ]
- Sung-Hwan, CHO; Il-Won, SEO; Jong-Duck, C.; In-Saeng, JOO Attività antimicrobica e antiossidante dell'estratto di pompelmo e semi sui prodotti della pesca. Korean J. Fish. Aquat. Sci. 1990 , 23, 289–296. [ Google Scholar ]
- Jong-Duck, C.; Il-Won, SEO; Sung-Hwan, CHO Studi sull'attività antimicrobica dell'estratto di semi di pompelmo. Korean J. Fish. Aquat. Sci. 1990 , 23, 297–302. [ Google Scholar ]
- Saaty, AH Attività antibatterica e antivirale degli estratti di semi di pompelmo: impatto del coronavirus 2 sulla sindrome respiratoria acuta grave. Arch. Pharm. Pract. 2022 , 13, 68–73. [ Google Scholar ] [ CrossRef ]
- Khaiat, A.; Saliou, C. Estratti botanici. In Cosmeceuticals and Active Cosmetics, 3a ed.; CRC Press: Boca Raton, FL, USA, 2015. [ Google Scholar ]
- Yarovaya, L.; Waranuch, N.; Wisuitiprot, W.; Khunkitti, W. Studio clinico sui cambiamenti della pelle asiatica dopo l'applicazione di una formulazione di protezione solare contenente estratto di semi d'uva. J. Cosmet. Dermatol. 2022 , 21, 4523–4535. [ Google Scholar ] [ CrossRef ]
- MTU. Politica etica della ricerca umana MTU. Disponibile online: https://www.mtu.ie/media/mtu-website/governance/policies-and-publications/academic-council-poli-cies-and-regulations/research-innovation-and-postgraduate-study/Human_Research_Ethics_Policy_AC_app_030622.pdf (consultato il 16 luglio 2024).
- Wood, K. Dichiarazione politica nazionale per garantire l'integrità della ricerca in Irlanda. Disponibile online: https://www.iua.ie/publications/national-policy-statement-on-ensuring-research-integrity-in-ireland/ (consultato il 5 settembre 2024).
Disclaimer/Nota dell'editore: le dichiarazioni, le opinioni e i dati contenuti in tutte le pubblicazioni appartengono esclusivamente ai singoli autori e collaboratori e non a MDPI e/o al/ai redattore/i. MDPI e/o il/i redattore/i declinano ogni responsabilità per eventuali danni a persone o proprietà derivanti da idee, metodi, istruzioni o prodotti a cui si fa riferimento nel contenuto.
© 2024 degli autori. Licenziatario MDPI, Basilea, Svizzera. Questo articolo è un articolo open access distribuito secondo i termini e le condizioni della licenza Creative Commons Attribution (CC BY) ( https://creativecommons.org/licenses/by/4.0/ ).
More on the Skincare Hub
View allPelle secca vs pelle disidratata: qual è la differenza e come prendersene cura?
Qual è la differenza e come prendersene cura?

irritazione da pannolino
L'eritema da pannolino è un problema comune a molti neonati, ma per un neo-genitore può essere spesso piuttosto angosciante vedere il proprio piccolo a disagio o irritato. Tuttavia, ci sono diversi accorgimenti che si possono adottare per prevenire e gestire l'eritema da pannolino. Qui rispondo ad alcune delle domande più comuni sull'eritema da pannolino, che spero possano esservi utili nella cura del vostro piccolo." – Dott.ssa Alexis Granite