Wybierz Region
-
Europe
-
Americas
-
Africa and Middle East
-
Asia Pacific
Arnold Marisa (1), Wisdom Shadrach (1), Kerrie Holohan (1), Abed Alkarem Abu Alhaija (2), Emer Gilligan (3), Jill Sommerville (3), Niall Burke (1) (*) i Tim Yeomans (1)
1 Shannon Applied Biotechnology Centre, Munster Technological University, V92 CX88 Tralee, Irlandia; [email protected] (WS); [email protected] (TY)
2 Oddział Biologi Jamy Ustnej, Szpital Stomatologiczny w Dublinie, Trinity College Dublin, D02 F859 Dublin, Irlandia
3 WaterWipes UC., Donore Road Industrial Estate, Donore Road, Rathmullan, A92 VX00 Drogheda, Irlandia; [email protected] (EG); [email protected] (JS)
*Korespondencja: [email protected]
Redaktor akademicki: Maria Manconi
Otrzymano zgłoszenie: 31 lipca 2024 r. / Zmieniono: 13 września 2024 r. / Zaakceptowano: 26 września 2024 r. / Opublikowano: 1 października 2024 r.
Abstrakcyjny
Kluczową funkcjonalnością chusteczek oczyszczających jest ich skuteczność w usuwaniu brudu i zanieczyszczeń mikrobiologicznych ze skóry do bezpiecznych lub niewykrywalnych poziomów, tradycyjnie określanych metodą wagową, która jest podatna na błędy eksperymentalne. W tym badaniu oceniano skuteczność chusteczek oczyszczających na bazie wody, WaterWipes® (WaterWipes, UC, Drogheda, Irlandia), w usuwaniu syntetycznych odchodów (Feclone™, SiliClone Creations LLC, Havertown, PA, Stany Zjednoczone) i Escherichia coli (NCTC 10538) ze skóry ochotników, przy czym w pierwszym przypadku zastosowano urządzenie do analizy skóry o nazwie kamera Antera 3D™ (Miravex Ltd., Dublin, Irlandia), a w drugim standardowe metody mikrobiologiczne. Feclone™ nałożono na przedramiona uczestników, a kamera Antera 3D™ uchwyciła szczegółowe obrazy powierzchni skóry przed i po przetarciu. Podejście z kamerą Antera 3D™ okazało się skuteczne w pomiarze skuteczności czyszczenia, a ściereczka usuwała wszystkie wykrywalne ślady zastosowanego Feclone™. Całkowita powierzchnia porów (mm2), liczba porów i całkowita objętość porów (mm3) u uczestników testu po przetarciu zmniejszyły się średnio odpowiednio o 39,05%, 34,39% i 39,98%. Ściereczka usunęła 99,99% zastosowanych bakterii E. coli (NCTC 10538), co zmierzono metodą mikrobiologiczną. Podsumowując, zaobserwowano, że metoda z kamerą Antera 3D™ okazała się skuteczna w ocenie usuwania miejscowo stosowanego Feclone™.
Słowa kluczowe: chusteczki oczyszczające; kamera Antera 3D™; Feclone™; WaterWipes®; usuwanie bakterii
1. Wprowadzenie
Chusteczki można opisać jako środki czyszczące i są one ogólnie podzielone na chusteczki suche i mokre, przy czym stosowanie chusteczek mokrych wzrosło w ostatnich latach, szczególnie w odniesieniu do higieny niemowląt i dzieci [ 1 ]. Badania pokazują, że stosowanie chusteczek mokrych poprawia wyniki czyszczenia pieluszek dziecięcych, zapewniając skuteczne czyszczenie i zmniejszając rumień skóry, odpowiednie zarówno dla nieuszkodzonych, jak i uszkodzonych powierzchni skóry w porównaniu do stosowania wody i tkaniny [ 2 , 3 , 4 , 5 ]. Chusteczki nawilżane dla niemowląt zazwyczaj składają się z materiałów bazowych w postaci arkusza opracowanych z łagodnym środkiem powierzchniowo czynnym czyszczącym, konserwantami i środkami buforującymi pH. Woda jest ogólnie stosowana jako składnik bazowy w chusteczkach dla niemowląt w celu czyszczenia wrażliwej skóry dzieci i pozostałości kału [ 4 , 6 ]. Europejskie spotkanie okrągłego stołu zaleciło, aby chusteczki nawilżane przeznaczone głównie do użytku przez dzieci nie miały potencjału wywoływania reakcji nadwrażliwości skóry i powinny być opracowane ze składników, które są bezpieczne do długotrwałego stosowania [ 7 ]. Chusteczki nawilżane przeznaczone do czyszczenia i dezynfekcji przechodzą standardowe testy, takie jak testy mikrobiologiczne, testy wydajności wycierania, testy wchłaniania wilgoci z chusteczek i testy formuły balsamu [ 1 ], przy czym skuteczność wycierania tradycyjnie określa się za pomocą metod wagowych (takich jak metoda odzyskiwania roztopionej czekolady), które, jak doniesiono, są podatne na błędy eksperymentalne [ 1 , 8 ].
W związku z tym w niniejszym badaniu starano się zaprojektować i ocenić nową, niegrawimetryczną metodę, która mogłaby znaleźć zastosowanie w przyszłości w ocenie skuteczności czyszczenia nowych i istniejących komercyjnych produktów do wycierania. Zaprojektowana metoda obejmuje użycie kamery Antera 3D™, znanej z obrazowania skóry w czasie rzeczywistym, z takimi zaletami, jak dostarczanie dokładnych, szybkich i obiektywnych danych w różnych obszarach badań skóry i oceny produktów kosmetycznych [ 9 , 10 , 11 , 12 ]. Kamera Antera 3D™ (Miravex Ltd., Dublin, Irlandia), objęta europejskim patentem nr 2400890, działa na zasadzie oświetlenia skóry pod wieloma kątami, a dane dotyczące powierzchni skóry są odtwarzane w sposób trójwymiarowy przy użyciu oprogramowania komputerowego w celu interpretacji odbitego światła od powierzchni skóry. Istotne dane dotyczące skóry, które można wygenerować za pomocą tego instrumentu, obejmują liczbę porów skóry, zmarszczki, szorstkość i analizę pigmentacji [ 13 ]. Pory skóry odgrywają rolę w uwalnianiu sebum, potu i resztek komórek ze skóry. Leczenie rozszerzonych porów twarzy (przy użyciu terapii z zastosowaniem ultradźwięków, światła szerokopasmowego, częstotliwości radiowej i frakcyjnych laserów nieablacyjnych) uznawane jest za wiodący trend w kosmetyce [ 14 ].
Opracowaną metodę oceniono przy użyciu WaterWipes® (WaterWipes UC, Drogheda, Irlandia), dostępnej w handlu marki chusteczek nawilżanych bez środków powierzchniowo czynnych, wyprodukowanych z minimalnej ilości składników. Jej podstawowy skład obejmuje materiały włókniste bez plastiku (zwilżone arkusze z włókniny, koronki przędzionej 100% wiskozy). Arkusze są zwilżane ultraoczyszczoną wodą (99,9%) i ekstraktem z nasion grejpfruta (Citrus grandis) 0,1% [ 15 ]. Jej skuteczność czyszczenia została przetestowana w porównaniu z miejscowymi aplikacjami FecloneTM i E. coli w dwóch oddzielnych badaniach z udziałem ochotników. FecloneTM (SiliClone Creations LLC, Havertown, PA, Stany Zjednoczone) to zastrzeżona marka sztucznego materiału symulującego kał, którego zastosowania zgłoszono w testach produktów spożywczych, a także chusteczek nawilżanych dla osób z nietrzymaniem moczu i niemowląt [ 16 , 17 ]. Do oceny skuteczności czyszczenia konkretnego, dostępnego w handlu produktu do ścierania w badaniu FecloneTM oraz metody liczenia płytek w badaniu E. coli zastosowano zaadaptowaną metodę kamery Antera 3DTM.
2. Materiały i metody
2.1. Ocena skuteczności czyszczenia produktem do ścierania w usuwaniu Feclone™
Badanie przeprowadzono na podstawie zgody etycznej wydanej przez Komitet ds. Etyki Badań nad Człowiekiem Uniwersytetu Technologicznego w Munster (HREC-FER-24-004) i zgodnie z normą BS EN 1500:2013 [ 1 ]. Kryteriami włączenia do badania byli mężczyźni i kobiety powyżej 18 roku życia ze zdrową, nieuszkodzoną i niewrażliwą skórą dorosłego człowieka, podczas gdy kryteriami wykluczenia byli dorośli wrażliwi, problemy skórne, wrażliwość skóry (samodzielnie zgłaszana) lub uszkodzona skóra na przedramieniu. Powstały panel składał się z 25 ochotników (18 kobiet i 7 mężczyzn); próbki i pobrane zdjęcia zostały zanonimizowane dla uczestników. Przedział wiekowy uczestników tego badania wynosił 18–50 lat. Badanie przeprowadzono w kontrolowanym środowisku w Shannon Applied Biotechnology Centre Laboratory (MTU, Kerry, Irlandia) w temperaturze otoczenia (25 ± 2 °C) i wilgotności względnej (50 ± 5%).
2.1.1. Przygotowanie Feclone™
Łącznie 120 ml wody destylowanej ogrzano do 99 °C w przykrytym naczyniu; jednocześnie 40 g Feclone™ wstępnie ogrzano przez 5 min za pomocą płyty grzejnej. Po osiągnięciu pożądanej temperatury podgrzaną wodę ostrożnie dodano do Feclone™ (SiliClone Creations LLC, Havertown, PA, USA), a następnie dokładnie mieszano przez około 20 s za pomocą szpatułki. Następnie mieszaninę przykryto folią aluminiową i inkubowano w temperaturze 99 °C przez co najmniej 30 min, przy czym mieszaninę delikatnie mieszano po pierwszych 10 min. Pod koniec okresu inkubacji wykonano ostatnie krótkie mieszanie przed alikwotowaniem gorącego roztworu do 50 ml probówek. Probówki umieszczono w temperaturze 4 °C do czasu dalszego użycia.
2.1.2. Zastosowanie Feclone™ na przedramieniu człowieka
Wolontariusze siedzieli z jedną ręką opartą o stół i odsłoniętym przedramieniem, pozwalając im na aklimatyzację do warunków pokojowych przez 3 minuty. Celem tego badania było określenie skuteczności czyszczenia chusteczki, dlatego temperatura skóry została uznana za mniej priorytetową. W obrębie sekcji o wymiarach 8 × 8 cm zabezpieczono obszar o wymiarach 4 × 4 cm, umieszczając szablon na przedramieniu wolontariusza. Ilość 2 g Feclone™ została nałożona na obszar o wymiarach 4 × 4 cm i równomiernie rozprowadzona za pomocą szpatułki. Procedura czyszczenia obejmowała wycieranie zanieczyszczonego obszaru w pionie i poziomie w następujący sposób: od lewej do prawej jedną powierzchnią chusteczki, następnie od prawej do lewej inną powierzchnią chusteczki, następnie od góry do dołu świeżą powierzchnią chusteczki i na koniec od dołu do góry nową powierzchnią chusteczki, wszystkie z tego samego arkusza.
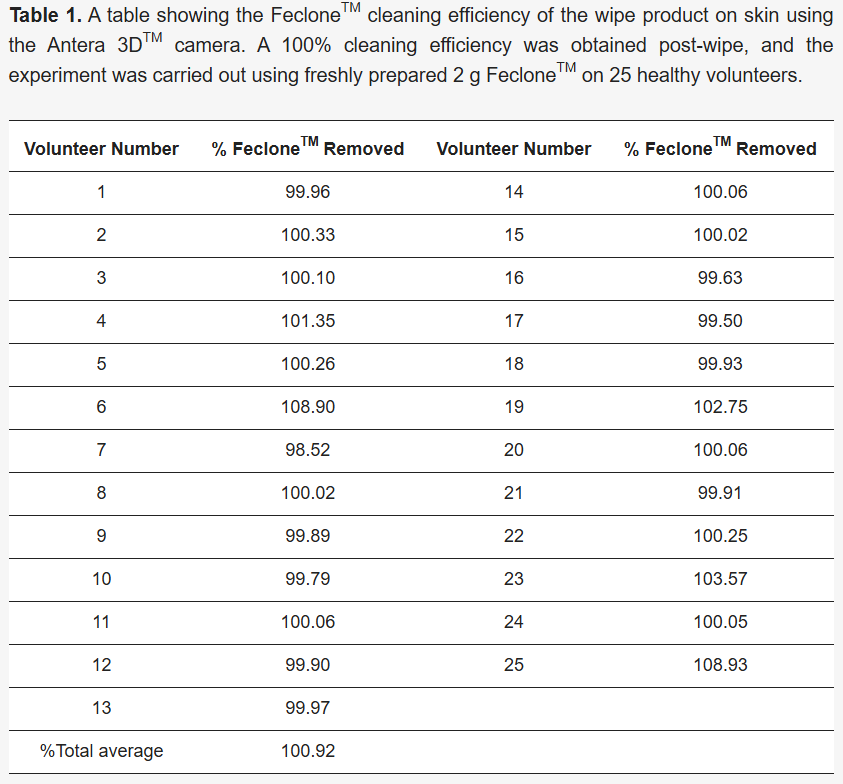
Obraz zaznaczonego obszaru został uchwycony za pomocą kamery Antera 3D™ przed i po czyszczeniu, a także bezpośrednio po zastosowaniu Feclone™, i przeanalizowany za pomocą oprogramowania Antera 3D™ (wersja 3.1.8) w celu porównania warunków przed i po wytarciu. Procent usunięcia został obliczony za pomocą parametru objętości oprogramowania, który mierzy zagłębienie i wzniesienie ponad znormalizowaną powierzchnię odniesienia. Objętość skóry (mm3) po wytarciu została odjęta od objętości skóry przed zastosowaniem FecloneTM; uzyskaną wartość odjęto od objętości skóry (mm3) po wstępnym wytarciu Feclone™ i podzielono przez objętość skóry (mm3) po wstępnym wytarciu Feclone™. Następnie wartość tę pomnożono przez 100 w celu obliczenia procentowego usunięcia (wzór w sekcji 3.1 ), a uzyskany wynik podano w sekcji 3.1 ( Tabela 1 ).
2.2. Ocena wpływu produktu do przecierania na pory skóry człowieka
Badanie przeprowadzono na gołym przedramieniu każdego ochotnika (w sumie 25). Obszar testowy oznaczono na ramieniu, jak opisano wcześniej, tak aby zdjęcia przed i po obejmowały dokładnie ten sam obszar. Następnie obszar sfotografowano, a następnie zastosowano 2 g Feclone™. Następną procedurę czyszczenia przeprowadzono zgodnie z opisem w sekcji 2.1.2 , a uzyskane wyniki można znaleźć w sekcji 3.2 ( Tabela 2 ). Wzór użyty dla różnych parametrów porów z oprogramowania Antera 3D™ (wersja 3.1.8) obejmuje:
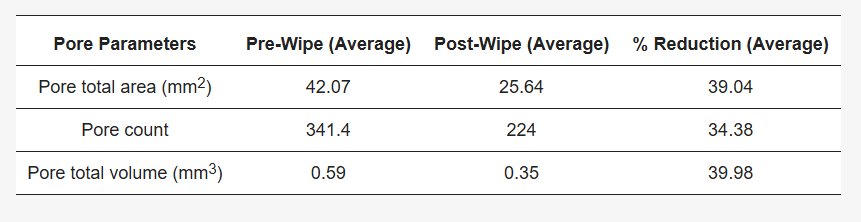
Tabela 2. Tabela pokazująca wpływ chusteczki testowej na pory skóry. Dane uzyskano i przeanalizowano przy użyciu metody kamery Antera 3D™. Po przetarciu zaobserwowano znaczącą redukcję średniej liczby porów, objętości i powierzchni w porównaniu z obrazowaniem tej samej powierzchni skóry przed przetarciem.
- Całkowita objętość porów (mm3) V = suma głębokości każdego piksela * powierzchnia piksela.
- Całkowita powierzchnia porów (mm2) = liczba pikseli wklęsłych * powierzchnia piksela.
- Liczba porów = izolowane wyspy depresyjne wewnątrz wybranego regionu zainteresowania.
2.3. Ocena skuteczności czyszczenia produktów do ścierania w przypadku bakterii E. Coli (NCTC 10538)
Badanie przeprowadzono przy użyciu KWIK STIK E. coli (NCTC 10538), pożywek bakteryjnych i 25 ochotników. Przygotowanie pożywek i kultur starterowych bakterii zostało przygotowane przed testowaniem na ochotnikach.
2.3.1. Kultura bakteryjna
Łącznie 30 g proszku Tryptone soya broth (TSB) dodano do 100 ml wody destylowanej. Mieszaninę dokładnie mieszano, aż proszek całkowicie się rozpuścił. Następnie objętość dostosowano wodą destylowaną do uzyskania objętości końcowej 1 l. Następnie podłoże wysterylizowano w autoklawie. Podłoże Tryptone soya agar (TSA) przygotowano w podobny sposób, ale używając 40 g/l proszku TSA.
Komórki Escherichia coli (E. coli) (NCTC 10538) początkowo zaszczepiono na płytkach TSA, a następnie umieszczono w inkubatorze ustawionym na 37 °C na noc. Następnego dnia wybrano pojedynczą kolonię i przeniesiono ją na inną płytkę TSA, którą następnie inkubowano w tych samych warunkach. Następnego dnia wybrano pojedynczą kolonię i wprowadzono ją do 10 ml pożywki TSB. Tę hodowlę inkubowano przez noc w temperaturze pokojowej z wytrząsaniem. Następnego dnia gęstość optyczną (OD) hodowli zmierzono za pomocą spektrofotometru, a komórki rozcieńczono pożywką TSB do osiągnięcia OD 0,15.
2.3.2. Zastosowanie bakterii na przedramieniu ochotników
Ta metoda została oparta na wytycznych określonych w normie BS EN 1500:2013 [ 1 ]. W całym eksperymencie konsekwentnie stosowano hodowle E. coli w bulionie o gęstości optycznej (OD) 0,15; średnia liczba użytych E. coli wynosiła 1,55 × 108 CFU/ml. Do zliczania metodą płytkową użyto alikwotu tej hodowli. Wolontariusze umyli ręce i ramiona mydłem nieantybakteryjnym, a następnie przetarli wymazem oczyszczony obszar, który umieszczono w 1 ml buforowanego fosforanem roztworu soli fizjologicznej (PBS) w celu zliczania metodą płytkową (służącą jako kontrola). Na skórze ochotnika zaznaczono obszar o wymiarach 4 × 4 cm do przeprowadzenia testu. Następnie 100 µl nocnej hodowli o OD 0,15 naniesiono pipetą na obszar testowy, delikatnie rozprowadzono za pomocą rozprowadzacza w kształcie litery L i pozostawiono do wyschnięcia na powietrzu przez 3 minuty.
Następnie wykonano procedurę czyszczenia przy użyciu chusteczki, jak opisano w rozdziale 2.1.2 . Użytą chusteczkę zanurzono w 10 ml neutralizującego medium Dey-Engley (D3435, Merck, Darmstadt, Niemcy), wirowano przez 60 s i rozcieńczano seryjnie dwukrotnie w medium PBS. Następnie 0,1 ml bakterii nałożono na płytkę agarową w celu przeprowadzenia hodowli przez noc i późniejszego kwantyfikacji. Po procesie przecierania powierzchnię obszaru testowego przedramienia przetarto zwilżonym wacikiem. Następnie wacik umieszczono w 1 ml medium PBS, a 0,1 ml nałożono na płytkę agarową w celu kwantyfikacji. Serie rozcieńczeń: czyste, 10−1 i 10−2 nałożono na płytkę agarową w celu kwantyfikacji w trzech powtórzeniach. Oryginalny zapas bakterii rozcieńczano seryjnie do 10−3, 10−4 i 10−5 i umieszczano na płytkach agarowych w celu zliczenia kolonii. Dla każdego obszaru CFU/ml obliczano przy użyciu następującego wzoru:
CFU/ml=(N ∗ DF)/VCCCFU/ml=(N ∗ DF)/VC
gdzie CFU/ml = jednostka tworząca kolonię na ml:
N = Liczba kolonii (całkowita liczba kolonii policzonych na płytkach w optymalnym zakresie).
DF = Współczynnik rozcieńczenia (odwrotność rozcieńczenia użytego do powlekania).
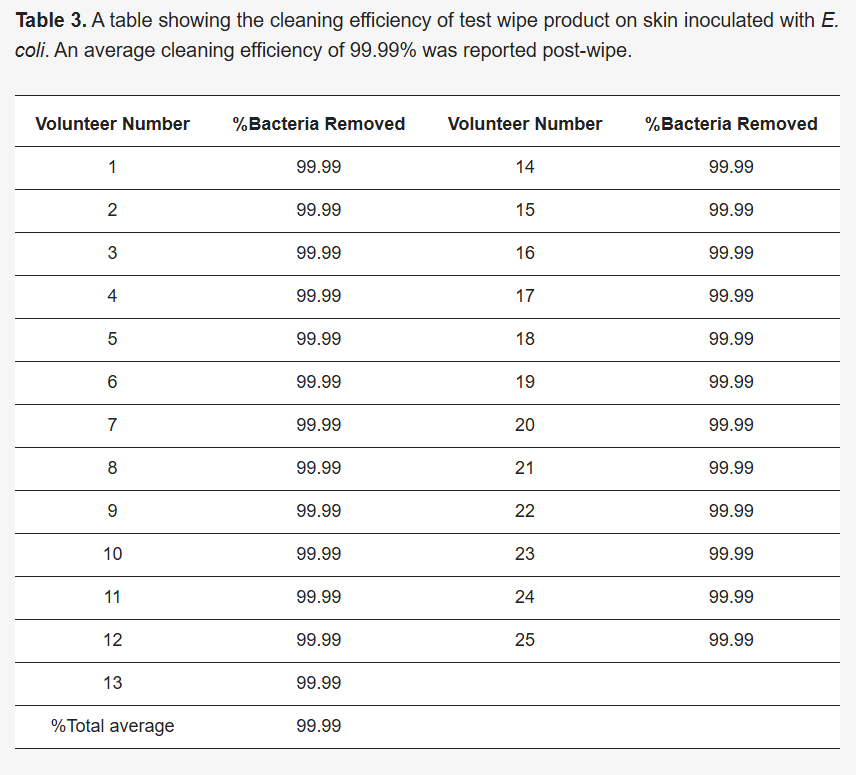
VC = Objętość hodowli wysianej (objętość rozcieńczonej hodowli wysianej na płytkę agarową). Tabelę pokazującą procent usuniętych bakterii można znaleźć w rozdziale 3.3 ( Tabela 3 ).
3. Wyniki
3.1. Ocena skuteczności czyszczenia produktu do wycierania w usuwaniu symulowanego materiału kałowego (Feclone™)
Zaadaptowana metoda Antera 3D™ została użyta do oceny skuteczności czyszczenia chusteczek testowych w zakresie usuwania Feclone™ z przedramion ochotników. Wyniki zostały przeanalizowane przy użyciu parametru objętości oprogramowania Antera 3D™. Objętość odnosi się do całkowitej grubości lub objętości wszelkich pozostałości lub zanieczyszczeń na powierzchni skóry, a zmniejszenie objętości po czyszczeniu wskazuje na skuteczne usunięcie (patrz Rysunek 1 ). Procent usunięcia obliczono przy użyciu następującego wzoru:
𝑠𝑣0−𝑠𝑣1⁄𝑠𝑣0×100sv0−sv1∕sv0×100
gdzie SV0 = Objętość skóry (mm3) z wstępnym przetarciem środkiem Feclone™.
SV1 = (Objętość skóry (mm3) po przetarciu — objętość skóry (mm3) przed zastosowaniem Feclone™).
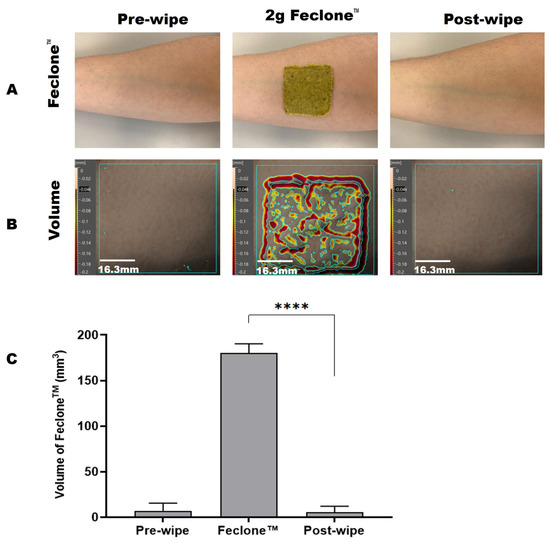
Rysunek 1. ( A ) Obrazy reprezentatywne przedstawiające ludzką skórę przedramienia przed i po nałożeniu i usunięciu Feclone™ za pomocą chusteczki testowej; obrazowanie wykonano za pomocą aparatu w telefonie. ( B ) Objętość Feclone™ wykryta na powierzchni skóry przedramienia za pomocą metody Antera 3D™ i czyszczenia chusteczką. Obszar zastosowania do analizy wynosił 40 mm × 40 mm. Pionowy pasek skali przedstawia objętość i topografię skóry, natomiast poziomy pasek skali odnosi się do pomiaru 2D określonego obszaru skóry. ( C ) Przedstawia objętości skóry przed przetarciem, Feclone™ i po przetarciu obserwowane za pomocą metody Antera 3DTM. Zaobserwowano, że chusteczka zmniejsza wzrost objętości skóry wywołany przez Feclone™ do poziomów sprzed aplikacji. Analiza sparowanego testu t podanej Feclone™ i resztkowej objętości skóry po przetarciu wykazała wysoce istotną różnicę (**** p < 0,0001). Wykres został przedstawiony jako średnia z SD (odchylenie standardowe) przy użyciu GraphPad Prism 10 (GraphPad Software, 225 Franklin Street, Fl. 26 Boston, MA 02110, USA). Stanowi to średnią skuteczność czyszczenia na poziomie 100,92%.
3.2. Ocena produktu do przecierania porów skóry człowieka
Po przetarciu skóry przedramienia ochotnika produktem do chusteczek zaobserwowano zmniejszenie parametrów porów, takich jak całkowita liczba porów, objętość porów i powierzchnia ( ryc. 2 ).
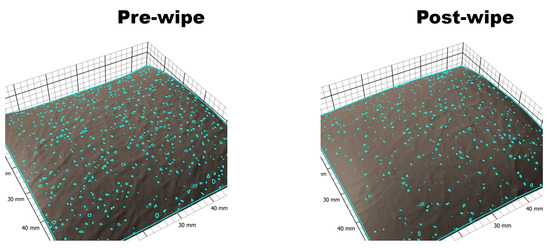
Rysunek 2. Przykładowy obraz z oprogramowania Antera 3DTM pokazujący zaobserwowaną redukcję widocznych porów skóry (liczba, powierzchnia całkowita, objętość całkowita) po oczyszczeniu za pomocą chusteczek.
3.3. Ocena skuteczności czyszczenia produktów do czyszczenia w usuwaniu bakterii E. Coli
Skuteczność produktu do ścierania w usuwaniu zanieczyszczeń bakteryjnych została również oceniona. Liczbę CFU/ml obliczono dla każdego obszaru i określono średnie. Wyniki te wskazują, że produkt do ścierania skutecznie usunął 99,99% komórek bakteryjnych i skutecznie oczyścił zanieczyszczone obszary skóry. Potwierdzono to poprzez zebranie zużytych chusteczek w celu ilościowego określenia bakterii po czyszczeniu, a także przetarcie czystego obszaru w celu przeprowadzenia hodowli na płytkach TSA (patrz rysunek 3 A, B).
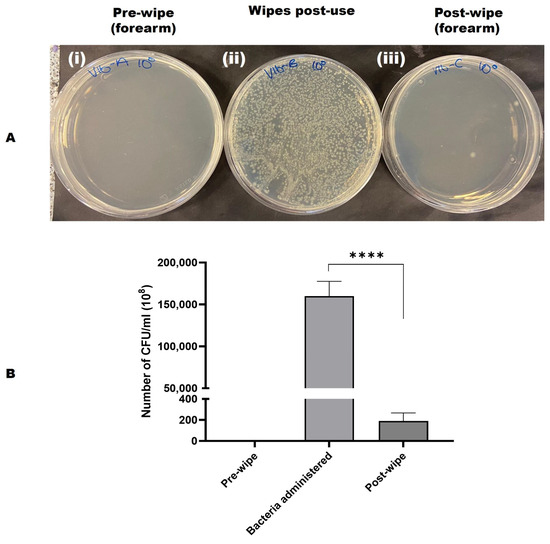
Rycina 3. ( A ) Obraz przedstawiający skuteczność usuwania bakterii przez chusteczki testowe z zanieczyszczonej skóry ludzkiej. ( i ) Wymazówka przed przetarciem pokryta powłoką ( ii ) Wymazówka pokryta powłoką ( iii ) Wymazówka po przetarciu pokryta powłoką. V = ochotnik, A = próbka przed przetarciem, B = wymazówka po użyciu, C = próbka po przetarciu, 100 = próbka czysta/nierozcieńczona. ( B ) Wykres skuteczności usuwania bakterii przez chusteczki przy użyciu E. coli i liczenia mikrobiologicznego. Zaobserwowano, że chusteczki testowe usunęły 99,99% bakterii z podanych. Analiza sparowanego testu t dla podanych bakterii i liczenia po przetarciu wykazała wysoce istotną różnicę (**** p < 0,0001). Wykres przedstawiono jako średnią z odchyleniem standardowym (SD) przy użyciu oprogramowania GraphPad Prism 10. V = ochotnik, A = próbka przed wytarciem, B = próbka po wytarciu, C = próbka po wytarciu, 100 = próbka czysta/nierozcieńczona.
4. Dyskusja
Celem tego badania było zaprojektowanie i ocena alternatywnej metody przeprowadzania badań skuteczności czyszczenia produktów chusteczkowych przy użyciu kamery Antera 3D™, urządzenia do obrazowania skóry i analizy. W tym badaniu wykorzystano dostępne w handlu chusteczki nawilżane dla niemowląt (WaterWipes®) i przetestowano ich skuteczność czyszczenia syntetycznymi odchodami (Feclone™) i zanieczyszczającymi bakteriami E. coli z powierzchni skóry przedramion ochotników. Kamera Antera 3D™, sprawdzone narzędzie do oceny produktów kosmetycznych [ 11 ], była stosowana w wielu badaniach kosmetycznych, takich jak te obejmujące ilościowe określanie zmarszczek, trądziku i pigmentacji [ 11 , 18 , 19 ], dlatego też opracowano i przetestowano adaptację europejskiej normy BS EN 1500:2013 [ 1 ] obejmującą kamerę Antera 3D™ do ilościowej i jakościowej oceny skuteczności czyszczenia chusteczek przy użyciu produktu chusteczkowego. Obiektywna analiza testu FecloneTM wykorzystała parametr głośności oprogramowania, aby zapewnić dogłębną ocenę skuteczności czyszczenia chusteczek.
Wyniki oceny wizualnej i analizy kamerą Antera 3D™ wykazały, że ta metoda była odpowiednia do oceny usuwania Feclone™ ze skóry człowieka za pomocą chusteczek, które wykazały 100,92% skuteczności czyszczenia Feclone™. Hipoteza, że wartość usuwania >100% może być spowodowana czułością metody kamery Antera 3D™ w wykrywaniu usuwania przez chusteczki zarówno nałożonego Feclone™, jak i wszelkich istniejących wcześniej zanieczyszczeń skóry. Podobne podejście obrazowania do określania skuteczności czyszczenia przez chusteczki zostało zgłoszone przez Lee i in. [ 8 ] i składa się z komputera ze skanerem i oprogramowaniem do analizy obrazu; jednak badanie to przeprowadzono przy użyciu zanieczyszczenia rozprowadzonego na płytce szklanej, a nie na skórze człowieka. Techniki obrazowania stanowią zatem alternatywę dla tradycyjnej metody wagowej stosowanej do oceny skuteczności czyszczenia chusteczek, która, jak donoszono, jest podatna na błędy eksperymentalne.
Metoda wagowa zazwyczaj obejmuje rejestrowanie ciężaru chusteczki przed i po przetarciu w celu określenia skuteczności czyszczenia. Ta technika koncentruje się na analizie chusteczki, a nie czyszczonej powierzchni. Zgłaszano, że metoda ta jest podatna na błędy, które mogą wynikać z procesu, takie jak obchodzenie się z chusteczkami podczas procesu ważenia, co może prowadzić do przenoszenia wilgoci z chusteczki na rękawiczki osoby przeprowadzającej test i nieuniknionego odparowania wilgoci z chusteczek testowych, co może mieć wpływ na uzyskane wyniki i powinno zostać uwzględnione jako zmienne eksperymentalne. Jednak w przypadku metody kamery Antera 3D™, która jest podejściem opartym na optyce, istnieje mniejsze ryzyko odparowania wilgoci z chusteczki i jej obchodzenia się, ponieważ skuteczność czyszczenia będzie wywnioskowana bezpośrednio z powierzchni skóry, a nie poprzez różnicę w ciężarze chusteczki, co sprawia, że ta metoda jest potencjalnie pomocna w radzeniu sobie z błędami powszechnymi w analizie wagowej. Inne zalety związane z proponowanymi metodami kamery Antera 3D™ obejmują jej zdolność do obrazowania skóry 3D, łatwość użytkowania, precyzję, powtarzalność i wielokrotny odczyt parametrów skóry, takich jak rozmiar porów, skazy, zmarszczki i szorstkość. Jednakże istnieją pewne ograniczenia zaobserwowane w przypadku proponowanych modeli, które obejmują niepewność co do ich stosowalności w innych obszarach charakterystyki skuteczności chusteczek nawilżanych, takich jak analiza szybkości suszenia chusteczek (szybkość odparowywania wilgoci z chusteczki po wystawieniu na działanie atmosfery w czasie), analiza pobierania chusteczek (zdolność mokrej chusteczki do pobierania balsamu) i badania transferu balsamu (uwalnianie balsamu z chusteczki na skórę) [ 1 , 8 , 20 ]. Ponieważ proponowana metoda wykorzystuje określone urządzenie, kamera Antera 3D™ i powiązane oprogramowanie są wymagane do wykonania lub odtworzenia metody, co stanowi potencjalne ograniczenie powszechnego zastosowania. Model jest techniką optyczną ze zmiennymi, takimi jak stała odległość, stopień rozdzielczości (0,1 mm) i pasmo widmowe (siedem) możliwe do uzyskania za pomocą kamery Antera 3D™, dzięki czemu zrekonstruowana topografia skóry staje się szacunkiem [ 21 ]. Czułość proponowanej techniki pozwala wykryć to, co znajduje się na skórze (włosy, pory, sebum, blizny, piegi itp.); nie oczekuje się jednak, że wpłynie to na generowane dane lub spowoduje artefakty, ponieważ protokół stanowi, że najpierw należy wykonać odczyty bazowe skóry.
Co ciekawe, zaobserwowano, że czyszczenie skóry za pomocą chusteczki ma wpływ na zmniejszenie całkowitej średniej liczby porów, objętości i powierzchni, co jest godne uwagi, ponieważ różne badania wykazały związek między mniejszą liczbą porów a zdrowszą skórą [ 14 , 22 , 23 ]. Jest to prawdopodobnie spowodowane połączeniem formulacji i składu chusteczki, w którym formulacja o niskim napięciu powierzchniowym rozprowadza i nawilża pory skóry wystarczająco, aby chusteczka mogła skutecznie oczyścić pory z sebum, potu i innych resztek komórek. Zmniejszenie średniej liczby i wielkości porów może być również wspomagane przez niższą temperaturę samych chusteczek. Temperatura chusteczek wydaje się niższa niż temperatura skóry; dlatego może to być powodem tymczasowego zamknięcia porów. Niektóre badania wykazały, że chłodzenie skóry prowadzi do zmniejszenia wielkości i liczby porów poprzez zwężenie naczyń krwionośnych skóry i jej naprężenie [ 24 , 25 , 26 ]. Ponadto ekstrakt z pestek grejpfruta (GSE), składnik kondycjonujący skórę i składnik używanego produktu chusteczkowego, ma właściwości przeciwdrobnoustrojowe [ 27 , 28 , 29 , 30 ]. Ma on również działanie antyoksydacyjne i pomaga złagodzić przekrwienie skóry poprzez oczyszczanie, odkażanie i udrażnianie zatkanych porów, zapewniając gładką i rozjaśnioną cerę, a także napinanie porów dzięki swoim właściwościom matującym [ 31 , 32 ]. Zaproponowano, że te chusteczki, WaterWipes® (WaterWipes UC, Drogheda, Irlandia), mogłyby znaleźć zastosowanie jako mniej inwazyjny sposób oczyszczania porów i minimalizowania ich widoczności, biorąc pod uwagę, że jako całość zmiana powierzchni, objętości i liczby porów po przetarciu może być kombinacją wszystkich powyższych powodów; jest to jednak osobny temat i konieczne jest przeprowadzenie dalszych badań w celu potwierdzenia tych ustaleń i określenia dokładnego mechanizmu działania, ponieważ w tym badaniu nie uwzględniono temperatur chusteczek i skóry ochotników. Niemniej jednak możliwości wizualizacji i pomiaru porów za pomocą kamery Antera 3D™ (Miravex Ltd., Dublin, Irlandia) pozwoliły na dodatkowe zrozumienie wpływu chusteczek na skórę.
5. Wnioski
Podsumowując, wyniki tego badania pokazują, że metoda kamery Antera 3D™ może być skuteczną alternatywną techniką oceny skuteczności chusteczek oczyszczających. Jej zalety obejmują prostotę użytkowania, powtarzalność danych, kontrolowane światło w wewnętrznym obszarze obrazu oraz fakt, że jest to przenośna jednostka o wysokiej rozdzielczości i wieloparametrowym odczycie. Jednakże, ponieważ nie przeprowadzono porównania z innymi metodami oceny skuteczności czyszczenia (takimi jak technika grawimetryczna), ta proponowana technika ma służyć jako potencjalna alternatywa dla istniejących metod. Stwierdzono, że produkt chusteczek używany w tym badaniu ma dobrą skuteczność czyszczenia w odniesieniu do znacznego usuwania zarówno Feclone™, jak i E. coli ze skóry człowieka. Dalsze badania mogą zbadać wydajność chusteczek na różnych typach skóry i częściach ciała oraz w różnych warunkach środowiskowych, aby poszerzyć ich zastosowanie i zrozumienie skuteczności przy użyciu opracowanej metody. Ogólnie rzecz biorąc, badanie to wnosi cenne spostrzeżenia na temat skuteczności metody kamery Antera 3D™ w zakresie pomiaru skuteczności czyszczenia chusteczek oczyszczających.
Wkład autorów
Konceptualizacja, TY, NB, JS i EG; metodologia, AAAA, AM; KH i NB; badania i analiza danych, AM, KH i WS; pisanie — przygotowanie oryginalnego projektu, WS; pisanie — recenzja i edycja, WS, NB, JS, EG i TY; zasoby, EG, JS i TY; nadzór, NB i TY; administracja i finansowanie projektu, TY, EG i JS Wszyscy autorzy przeczytali i zaakceptowali opublikowaną wersję manuskryptu.
Finansowanie
Badania te zostały dofinansowane przez WaterWipes UC.
Oświadczenie Rady ds. Przeglądu Instytucjonalnego
To badanie z udziałem ochotników przeprowadzono zgodnie z Deklaracją Helsińską i zatwierdzono przez Komitet ds. Etyki Badań na Ludziach Uniwersytetu Technologicznego w Munster (nr referencyjny MTU-HREC-FER-24-004). Zarządzanie Komitetem ds. Etyki Badań na Ludziach Uniwersytetu Technologicznego w Munster jest zgodne z Polityką Etyki Badań na Ludziach Uniwersytetu [ 33 ] i jest zgodne z Krajowym Oświadczeniem Politycznym w sprawie Zapewnienia Integralności Badań w Irlandii (Narodowe Forum Integralności Badań (2019) [ 34 ]. Wszelka działalność badawcza, w której uczestniczą ludzie, musi przejść formalną kontrolę etyczną przed rozpoczęciem.
Oświadczenie o świadomej zgodzie
Wszyscy ochotnicy wyrazili świadomą zgodę na piśmie przed wzięciem udziału w badaniu.
Oświadczenie o dostępności danych
Wszystkie dane można znaleźć w tym artykule.
Podziękowanie
Wszyscy ochotnicy biorący udział w obu badaniach zostali docenieni za swój udział w zbieraniu danych.
Konflikty interesów
Autorzy Jill Sommerville i Emer Gilligan byli zatrudnieni przez firmę WaterWipes UC. Pozostali autorzy oświadczają, że badania przeprowadzono w nieobecności jakichkolwiek powiązań komercyjnych lub finansowych, które można by uznać za potencjalny konflikt interesów.
Odniesienia
- Cheriaa, R.; Boubaker, J. Ocena jakości nawilżanych chusteczek dla niemowląt. J. Ind. Tekst. 2022 , 51, 2124S–2147S. [ Google Scholar ] [ CrossRef ]
- Visscher, M.; Odio, M.; Taylor, T.; White, T.; Sargent, S.; Sluder, L.; Smith, L.; Flower, T.; Mason, B.; Rider, M.; i in. Pielęgnacja skóry u pacjentów oddziału intensywnej terapii noworodków: wpływ chusteczek w porównaniu z tkaniną i wodą na integralność warstwy rogowej. Neonatology 2009 , 96, 226–234. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Garcia Bartels, N.; Massoudy, L.; Scheufele, R.; Dietz, E.; Proquitté, H.; Wauer, R.; Bertin, C.; Serrano, J.; Blume-Peytavi, U. Standaryzowany schemat pielęgnacji pieluszek: prospektywne, randomizowane badanie pilotażowe dotyczące funkcji bariery skórnej i naskórkowego IL-1α u noworodków. Pediatr. Dermatol. 2012 , 29, 270–276. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Rodriguez, KJ; Cunningham, C.; Foxenberg, R.; Hoffman, D.; Vongsa, R. Nauka stojąca za chusteczkami nawilżanymi do skóry niemowląt: przegląd składników, bezpieczeństwo i skuteczność. Pediatr. Dermatol. 2020 , 37, 447–454. [ Google Scholar ] [ CrossRef ]
- Odio, M.; Streicher-Scott, J.; Hansen, RC Jednorazowe chusteczki nawilżane dla dzieci: skuteczność i łagodność dla skóry. Dermatol. Nurs. 2001 , 13, 107–112, 117–118, 121. [ Google Scholar ]
- Ehretsmann, C.; Schaefer, P.; Adam, R. Tolerancja skórna chusteczek nawilżanych przez niemowlęta z atopowym zapaleniem skóry i porównanie łagodności chusteczek nawilżanych i wody dla skóry niemowląt. J. Eur. Acad. Dermatol. Venereol. 2001 , 15, 16–21. [ Google Scholar ] [ CrossRef ]
- Blume-Peytavi, U.; Lavender, T.; Jenerowicz, D.; Ryumina, I.; Stalder, J.; Torrelo, A.; Cork, MJ Zalecenia z europejskiego okrągłego stołu na temat najlepszych praktyk w zakresie pielęgnacji zdrowej skóry niemowląt. Pediatr. Dermatol. 2016 , 33, 311–321. [ Google Scholar ] [ CrossRef ]
- Lee, J.; Kim, S.; Oh, KW Analiza obrazu: nowa technika określania skuteczności ściereczek do wycierania. Fibers Polym. Fiber Polym. 2006 , 7, 73–78. [ Google Scholar ] [ CrossRef ]
- Kandil, SM; Soliman, II; Diab, HM; Bedair, NI; Mahrous, MH; Abdou, EM Pęcherzykowe nośniki fosforanu askorbylu magnezu do stosowania miejscowego; przygotowanie, ocena in vitro i ex vivo, optymalizacja czynnikowa i ocena kliniczna u pacjentów z melasmą. Drug Deliv. 2022 , 29, 534–547. [ Google Scholar ] [ CrossRef ]
- Prendergast, PM Obrazowanie skóry w medycynie estetycznej. W Medycyna estetyczna: sztuka i techniki; Prendergast, PM, Shiffman, MA, red.; Springer: Berlin/Heidelberg, Niemcy, 2012; s. 59–68. ISBN 978-3-642-20113-4. [ Google Scholar ]
- Messaraa, C.; Metois, A.; Walsh, M.; Hurley, S.; Doyle, L.; Mansfield, A.; O'Connor, C.; Mavon, A. Pomiar zmarszczek i szorstkości za pomocą Antera 3D i jego zastosowanie do oceny produktów kosmetycznych. Skin Res. Technol. 2018 , 24, 359–366. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Francesco, A. Prospektywne, randomizowane badanie kliniczne nowej miejscowej formulacji do redukcji zmarszczek na twarzy i regeneracji skóry właściwej. J. Cosmet. Dermatol. 2021 , 20, 2832–2840. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Anqi, S.; Xiukun, S.; Ai'e, X. Ilościowa ocena wrażliwej skóry za pomocą ANTERA 3D® w połączeniu z GPSkin Barrier®. Skin Res. Technol. 2022 , 28, 840–845. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Parvar, SY; Amani, M.; Shafiei, M.; Rastaghi, F.; Hosseini, SA; Ahramiyanpour, N. Skuteczność i skutki uboczne opcji leczenia porów twarzy: artykuł przeglądowy. J. Cosmet. Dermatol. 2023 , 22, 763–775. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- WaterWipe. Nasza historia chusteczek nawilżanych dla dzieci|WaterWipes UK. WaterWipes. Dostępne online: https://www.waterwipes.com/uk/en/our-story (dostęp 12 lipca 2024).
- Marsh, RG; Miller, KH; Dannenberg, A. Metoda oceny przylegania gleb lub wysięków do skóry. US20100228107A1, 9 września 2010. Dostępne online: https://patents.google.com/patent/US20100228107A1/en (dostęp: 3 lipca 2024).
- Jubinville, E.; Girard, M.; Trudel-Ferland, M.; Fliss, I.; Jean, J. Inaktywacja mysiego norowirusa zawieszonego w materii organicznej symulująca rzeczywiste warunki skażenia wirusowego. Food Environ. Virol. 2021 , 13, 544–552. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Araco, F. Wstępne prospektywne i randomizowane badanie wysoko oczyszczonego polinukleotydu w porównaniu z placebo w leczeniu umiarkowanych do ciężkich blizn potrądzikowych. Aesthet. Surg. J. 2021 , 41, NP866–NP874. [ Google Scholar ] [ CrossRef ]
- Niemeyer-van der Kolk, T.; Buters, TP; Krouwels, L.; Boltjes, J.; de Kam, ML; van der Wall, H.; van Alewijk, DCJG; van den Munckhof, EHA; Becker, MJ; Feiss, G.; i in. Miejscowy peptyd przeciwdrobnoustrojowy omiganan przywraca dysbiozę skóry, ale nie poprawia objawów klinicznych u pacjentów z łagodnym do umiarkowanego atopowym zapaleniem skóry w randomizowanym badaniu kontrolowanym fazy 2 .
- Hossain, MM; Jones, JM; Dey, S.; Carr, GJ; Visscher, MO Ilościowe oznaczanie przenikania balsamu z chusteczek nawilżanych do skóry wcześniaków i noworodków. Food Chem. Toxicol. 2015 , 84, 106–114. [ Google Scholar ] [ CrossRef ]
- Gitlina, Y.; Guarnera, GC; Dhillon, DS; Hansen, J.; Lattas, A.; Pai, D.; Ghosh, A. Praktyczny pomiar i rekonstrukcja odbicia widmowego skóry. Comput. Graph. Forum 2020 , 39, 75–89. [ Google Scholar ] [ CrossRef ]
- Messaraa, C.; Metois, A.; Walsh, M.; Flynn, J.; Doyle, L.; Robertson, N.; Mansfield, A.; O'Connor, C.; Mavon, A. Możliwości 3D Antera do pomiaru porów. Skin Res. Technol. 2018 , 24, 606–613. [ Google Scholar ] [ CrossRef ]
- Vachiramon, V.; Namasondhi, A.; Anuntrangsee, T.; Kositkuljorn, C.; Jurairattanaporn, N. Badanie skojarzonych mikrofokusowanych ultradźwięków i wypełniaczy skórnych na bazie kwasu hialuronowego w leczeniu rozszerzonych porów twarzy u Azjatów. J. Cosmet. Dermatol. 2021 , 20, 3467–3474. [ Google Scholar ] [ CrossRef ]
- Shahzad, Y.; Louw, R.; Gerber, M.; du Plessis, J. Przełamywanie bariery skórnej poprzez modulację temperatury. J. Control. Wydanie 2015 , 202, 1–13. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Johnson, JM; Kellogg, DL Lokalna kontrola termiczna krążenia skórnego u człowieka. J. Appl. Physiol. 2010 , 109, 1229–1238. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Charkoudian, N. Przepływ krwi przez skórę w termoregulacji u dorosłych ludzi: jak działa, kiedy nie działa i dlaczego. Mayo Clin. Proc. 2003 , 78, 603–612. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Park, H.-K.; Kim, S.-B. Aktywność przeciwdrobnoustrojowa ekstraktu z pestek grejpfruta. Korean J. Food Nutr. 2006 , 19, 526–531. [ Google Scholar ]
- Sung-Hwan, CHO; Il-Won, SEO; Jong-Duck, C.; In-Saeng, JOO Aktywność przeciwbakteryjna i antyoksydacyjna ekstraktu z grejpfruta i nasion w produktach rybołówstwa. Korean J. Fish. Aquat. Sci. 1990 , 23, 289–296. [ Google Scholar ]
- Jong-Duck, C.; Il-Won, SEO; Sung-Hwan, CHO Badania nad aktywnością przeciwdrobnoustrojową ekstraktu z pestek grejpfruta. Korean J. Fish. Aquat. Sci. 1990 , 23, 297–302. [ Google Scholar ]
- Saaty, AH Aktywność przeciwbakteryjna i przeciwwirusowa ekstraktów z pestek grejpfruta: wpływ na zespół ostrej niewydolności oddechowej wywołany koronawirusem 2. Arch. Pharm. Pract. 2022 , 13, 68–73. [ Google Scholar ] [ CrossRef ]
- Khaiat, A.; Saliou, C. Ekstrakty botaniczne. W Cosmeceuticals and Active Cosmetics, 3. wyd.; CRC Press: Boca Raton, FL, USA, 2015. [ Google Scholar ]
- Yarovaya, L.; Waranuch, N.; Wisuitiprot, W.; Khunkitti, W. Badanie kliniczne zmian skórnych Azjatów po zastosowaniu preparatu z filtrem przeciwsłonecznym zawierającego ekstrakt z pestek winogron. J. Cosmet. Dermatol. 2022 , 21, 4523–4535. [ Google Scholar ] [ CrossRef ]
- MTU. Polityka etyki badań na ludziach MTU. Dostępne online: https://www.mtu.ie/media/mtu-website/governance/policies-and-publications/academic-council-poli-cies-and-regulations/research-innovation-and-postgraduate-study/Human_Research_Ethics_Policy_AC_app_030622.pdf (dostęp 16 lipca 2024).
- Wood, K. National Policy Statement on Ensuring Research Integrity in Ireland. Dostępne online: https://www.iua.ie/publications/national-policy-statement-on-ensuring-research-integrity-in-ireland/ (dostęp 5 września 2024).
Zastrzeżenie/Uwaga wydawcy: Oświadczenia, opinie i dane zawarte we wszystkich publikacjach są wyłącznie opiniami poszczególnych autorów i współpracowników, a nie MDPI i/lub redaktorów. MDPI i/lub redaktorzy nie ponoszą odpowiedzialności za jakiekolwiek obrażenia osób lub szkody materialne wynikające z jakichkolwiek pomysłów, metod, instrukcji lub produktów, do których odnoszą się treści.
© 2024 by the authors. Licenseee MDPI, Basel, Switzerland. Niniejszy artykuł jest artykułem o otwartym dostępie rozpowszechnianym na warunkach licencji Creative Commons Attribution (CC BY) ( https://creativecommons.org/licenses/by/4.0/ ).
More on the Skincare Hub
View allSkóra sucha a odwodniona: jaka jest różnica i jak o nią dbać?
Jaka jest różnica i jak o nią dbać?

Odparzenia pieluszkowe
Odparzenia pieluszkowe to częsty problem, z którym zmaga się wiele niemowląt, ale dla świeżo upieczonego rodzica widok dyskomfortu lub podrażnienia u maluszka może być często bardzo przygnębiający. Istnieje jednak szereg kroków, które można podjąć, aby zapobiec odparzeniom pieluszkowym i sobie z nimi radzić. Poniżej odpowiadam na kilka najczęściej zadawanych pytań dotyczących odparzeń pieluszkowych, które, mam nadzieję, pomogą Ci w opiece nad Twoim maluszkiem. – Dr Alexis Granite