Sélectionner une Région
-
Europe
-
Americas
-
Africa and Middle East
-
Asia Pacific
Arnold Marisa (1) , Wisdom Shadrach (1) , Kerrie Holohan (1) , Abed Alkarem Abu Alhaija (2) , Emer Gilligan (3) , Jill Sommerville (3) , Niall Burke (1) (*) et Tim Yeomans (1)
1 Centre de biotechnologie appliquée de Shannon, Université technologique de Munster, V92 CX88 Tralee, Irlande ; [email protected] (WS) ; [email protected] (TY)
2 Division de biosciences orales, Hôpital dentaire de Dublin, Trinity College Dublin, D02 F859 Dublin, Irlande
3 WaterWipes UC., Donore Road Industrial Estate, Donore Road, Rathmullan, A92 VX00 Drogheda, Irlande ; [email protected] (EG) ; [email protected] (JS)
*Correspondance : [email protected]
Rédactrice académique : Maria Manconi
Soumission reçue : 31 juillet 2024 / Révisée : 13 septembre 2024 / Acceptée : 26 septembre 2024 / Publiée : 1er octobre 2024
Abstrait
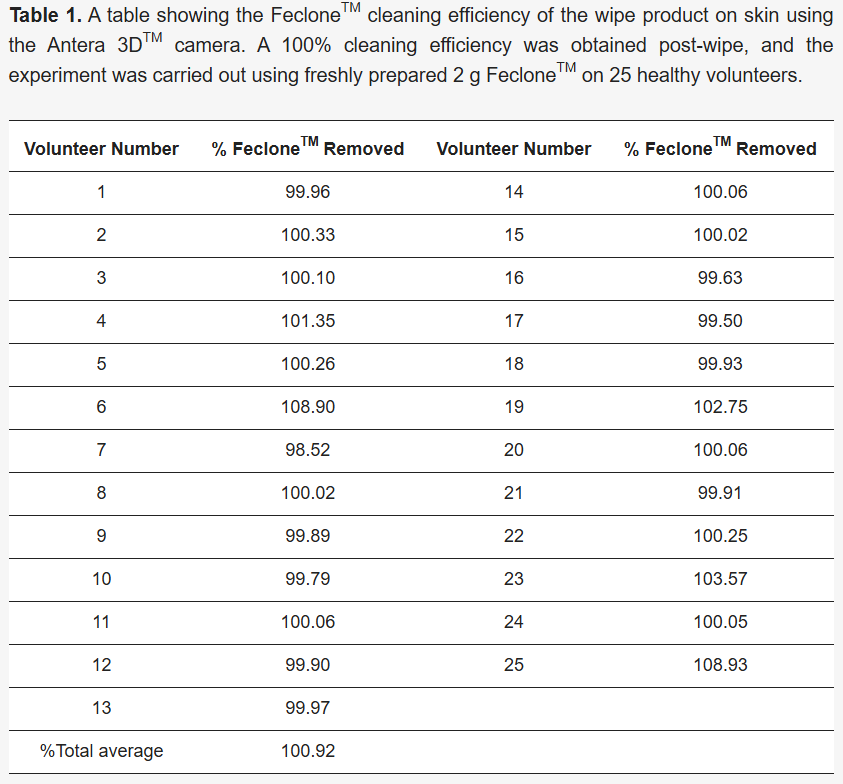
L'une des principales caractéristiques des lingettes nettoyantes est leur efficacité à éliminer les impuretés et la contamination microbienne de la peau jusqu'à des niveaux sûrs, voire indétectables. Ces niveaux sont traditionnellement déterminés par la méthode gravimétrique, dont la sensibilité aux erreurs expérimentales est avérée. Cette étude évalue l'efficacité d'une lingette nettoyante à base d'eau, WaterWipes® (WaterWipes, UC, Drogheda, Irlande), pour éliminer les matières fécales synthétiques (Feclone™, SiliClone Creations LLC, Havertown, PA, États-Unis) et Escherichia coli (NCTC 10538) de la peau de volontaires. La première a été réalisée à l'aide d'un appareil d'analyse cutanée appelé caméra Antera 3D™ (Miravex Ltd., Dublin, Irlande), et la seconde à l'aide de méthodes microbiologiques standard. La Feclone™ a été appliquée sur les avant-bras des participants et la caméra Antera 3D™ a capturé des images détaillées de la surface cutanée avant et après l'essuyage. L'approche par caméra Antera 3D™ s'est avérée efficace pour mesurer l'efficacité du nettoyage, la lingette éliminant toute trace détectable de Feclone™ appliqué. Après essuyage, la surface totale des pores (mm²), le nombre de pores et le volume total des pores (mm³) des participants ont été réduits en moyenne de 39,05 %, 34,39 % et 39,98 % respectivement. La lingette a éliminé 99,99 % des E. coli (NCTC 10538) appliqués, selon la méthode de numération microbienne sur plaque. En conclusion, la méthode par caméra Antera 3D™ s'est avérée efficace pour évaluer l'élimination du Feclone™ appliqué localement.
Mots-clés : lingettes nettoyantes ; caméra Antera 3D™ ; Feclone™ ; WaterWipes® ; élimination bactérienne
1. Introduction
Les lingettes peuvent être décrites comme des agents nettoyants et sont généralement divisées en lingettes sèches et humides, l'utilisation de lingettes humides ayant augmenté ces dernières années, notamment pour l'hygiène des bébés et des nourrissons [ 1 ]. Des études montrent que l'utilisation de lingettes humides améliore les résultats du nettoyage des couches de bébé, offrant un nettoyage efficace et réduisant l'érythème cutané, convenant aux surfaces cutanées intactes et altérées par rapport à l'utilisation d'eau et de tissu [ 2 , 3 , 4 , 5 ]. Les lingettes humides pour bébé sont généralement constituées de matériaux en feuille formulés avec un tensioactif nettoyant doux, des conservateurs et des agents tampons de pH. L'eau est généralement utilisée comme composant de base dans les lingettes pour bébé afin de nettoyer la peau sensible des bébés et les résidus fécaux [ 4 , 6 ]. Il a été recommandé lors d'une table ronde européenne que les lingettes humides conçues principalement pour les bébés ne soient pas susceptibles de provoquer des réactions de sensibilité cutanée et soient formulées avec des ingrédients sûrs pour une utilisation à long terme [ 7 ]. Les lingettes humides conçues pour les applications de nettoyage et de désinfection sont soumises à des tests standard, tels que des tests microbiologiques, l'efficacité d'essuyage, la récupération de l'humidité des lingettes et la formulation de lotion [ 1 ], l'efficacité d'essuyage étant traditionnellement déterminée à l'aide de méthodes gravimétriques de nettoyage par essuyage (telles que la technique de récupération du chocolat fondu) qui se sont avérées sujettes à des erreurs expérimentales [ 1 , 8 ].
Par conséquent, cette étude vise à concevoir et à évaluer une nouvelle méthode non gravimétrique potentiellement utile pour évaluer l'efficacité nettoyante des lingettes commerciales nouvelles et existantes. La méthode conçue implique l'utilisation d'une caméra Antera 3D™ connue pour son imagerie dermique en temps réel, avec des avantages tels que la fourniture de données précises, rapides et objectives dans différents domaines des études cutanées et de l'évaluation des produits cosmétiques [ 9 , 10 , 11 , 12 ]. La caméra Antera 3D™ (Miravex Ltd., Dublin, Irlande), sous le brevet européen n° 2400890, fonctionne sur le principe de l'illumination de la peau sous plusieurs angles, les données de surface cutanée étant reproduites en 3D à l'aide d'un logiciel informatisé pour interpréter la lumière réfléchie par la surface de la peau. Les données cutanées pertinentes qui peuvent être générées avec cet instrument comprennent le nombre de pores cutanés, les rides, la rugosité et l'analyse de la pigmentation [ 13 ]. Les pores de la peau jouent un rôle dans l'élimination du sébum, de la sueur et des débris cellulaires. Le traitement des pores dilatés du visage (par des thérapies telles que les ultrasons, la lumière à large bande, la radiofréquence et les lasers fractionnés non ablatifs) est considéré comme une demande cosmétique majeure [ 14 ].
La méthode conçue a été évaluée à l'aide de WaterWipes® (WaterWipes UC, Drogheda, Irlande), une marque commerciale de lingettes humides sans tensioactifs fabriquées avec un minimum d'ingrédients. Sa composition de base comprend des matériaux fibreux sans plastique (feuilles humidifiées de tissu non tissé filé en dentelle 100 % viscose). Les feuilles sont humidifiées avec de l'eau ultra-purifiée (99,9 %) et de l'extrait de pépins de citrus grandis (pamplemousse) à 0,1 % [ 15 ]. Son efficacité nettoyante a été testée par application topique de FecloneTM et d'E. coli dans deux essais distincts sur des volontaires humains. FecloneTM (SiliClone Creations LLC, Havertown, PA, États-Unis) est une marque déposée de matière fécale artificielle simulée dont les applications ont été signalées dans les tests de produits alimentaires ainsi que de lingettes pour l'incontinence et les lingettes pour bébés [ 16 , 17 ]. La méthode de caméra Antera 3DTM adaptée a été utilisée pour évaluer l'efficacité de nettoyage d'un produit d'essuyage spécifique disponible dans le commerce dans l'essai FecloneTM et la méthode de comptage des plaques pour l'essai E. coli.
2. Matériels et méthodes
2.1. Évaluation de l'efficacité du produit de nettoyage par lingettes pour éliminer le Feclone™
Français Cette étude a été menée sur la base de l'approbation éthique du Comité d'éthique de la recherche humaine de l'Université technologique de Munster (HREC-FER-24-004) et a fonctionné conformément à la norme BS EN 1500:2013 [ 1 ]. Les critères d'inclusion pour l'étude étaient les hommes et les femmes de plus de 18 ans avec une peau humaine adulte saine, intacte et non sensible, tandis que les critères d'exclusion étaient les adultes vulnérables, les plaintes cutanées, la sensibilité cutanée (autodéclarée) ou la peau lésée sur l'avant-bras. Le panel résultant était composé de 25 volontaires humains (18 femmes et 7 hommes) ; les échantillons et les images prises ont été anonymisés pour les participants. La tranche d'âge des participants à cette étude était de 18 à 50 ans. L'enquête a été menée dans un environnement contrôlé au laboratoire du Shannon Applied Biotechnology Centre (MTU, Kerry, Irlande) avec une température ambiante (25 ± 2 °C) et une humidité relative (50 ± 5 %).
2.1.1. Préparation de Feclone™
Au total, 120 ml d'eau distillée ont été chauffés à 99 °C dans un récipient fermé ; simultanément, 40 g de Feclone™ ont été préchauffés pendant 5 minutes à l'aide d'une plaque chauffante. Une fois la température souhaitée atteinte, l'eau chauffée a été soigneusement ajoutée au Feclone™ (SiliClone Creations LLC, Havertown, PA, États-Unis), puis le mélange a été agité vigoureusement pendant environ 20 secondes à l'aide d'une spatule. Le mélange a ensuite été recouvert d'une feuille d'aluminium et incubé à 99 °C pendant au moins 30 minutes, puis agité doucement après les 10 premières minutes. À la fin de l'incubation, une dernière brève agitation a été effectuée avant de répartir la solution chaude dans des tubes de 50 ml. Les tubes ont été placés à 4 °C jusqu'à leur utilisation.
2.1.2. Application de Feclone™ sur l'avant-bras humain
Les volontaires étaient assis, un bras posé sur une table, l'avant-bras exposé, et pouvaient s'acclimater aux conditions ambiantes pendant 3 minutes. L'objectif de cette étude était de déterminer l'efficacité nettoyante de la lingette ; la température cutanée était donc considérée comme une priorité secondaire. Sur une section de 8 × 8 cm, une zone de 4 × 4 cm a été délimitée en plaçant un gabarit sur l'avant-bras du volontaire. Une dose de 2 g de Feclone™ a été appliquée sur cette zone et répartie uniformément à l'aide d'une spatule. La procédure de nettoyage consistait à essuyer la zone contaminée verticalement et horizontalement comme suit : de gauche à droite avec une lingette, puis de droite à gauche avec une autre lingette, puis de haut en bas avec une lingette neuve, et enfin de bas en haut avec une nouvelle lingette, le tout à partir de la même feuille.
Une image de la zone marquée a été capturée à l'aide d'une caméra Antera 3D™ avant et après le nettoyage, ainsi qu'immédiatement après l'application de Feclone™, puis analysée à l'aide du logiciel Antera 3D™ (version 3.1.8) afin de comparer les conditions avant et après l'essuyage. Le pourcentage d'élimination a été calculé à l'aide du paramètre de volume du logiciel, qui mesure la dépression et l'élévation au-dessus d'une surface de référence normalisée. Le volume cutané (mm³) après l'essuyage a été soustrait du volume cutané avant l'application de Feclone™ ; la valeur obtenue a été soustraite du volume cutané (mm³) avec Feclone™ avant l'essuyage et divisée par le volume cutané (mm³) avec Feclone™ avant l'essuyage. Cette valeur a ensuite été multipliée par 100 pour calculer le pourcentage d'élimination (formule de la section 3.1 ) ; le résultat obtenu est présenté à la section 3.1 ( tableau 1 ).
2.2. Évaluation de l'impact des lingettes sur les pores de la peau humaine
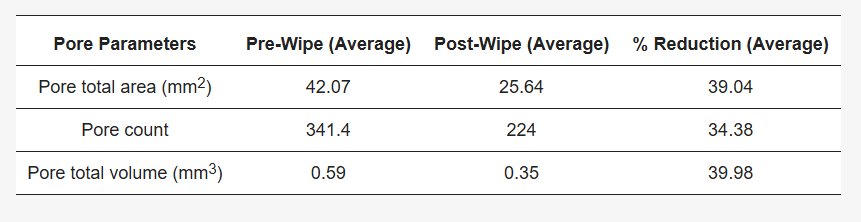
Cette étude a été réalisée sur l'avant-bras nu de chaque volontaire (25 au total). La zone de test a été délimitée sur le bras comme décrit précédemment, de sorte que les photos avant et après soient exactement identiques. La zone a ensuite été photographiée, puis 2 g de Feclone™ ont été appliqués. Le nettoyage ultérieur a été effectué comme décrit à la section 2.1.2 et les résultats obtenus sont présentés à la section 3.2 ( tableau 2 ). La formule utilisée pour les différents paramètres des pores, issue du logiciel Antera 3D™ (version 3.1.8), comprend :
Tableau 2. Tableau montrant l'impact de la lingette test sur les pores de la peau. Les données ont été obtenues et analysées à l'aide de la méthode de la caméra Antera 3D™. Une réduction significative du nombre moyen de pores, de leur volume et de leur surface a été observée après l'essuyage, par rapport à l'imagerie de la même surface cutanée avant l'essuyage.
- Volume total des pores (mm3) V = somme de la profondeur pour chaque pixel * surface du pixel.
- Surface totale des pores (mm2) = nombre de pixels enfoncés * surface des pixels.
- Nombre de pores = îlots de dépression isolés à l'intérieur de la région d'intérêt sélectionnée.
2.3. Évaluation de l'efficacité des lingettes nettoyantes contre E. coli (NCTC 10538)
Cette étude a été menée à l'aide de la souche KWIK STIK E. coli (NCTC 10538), de milieux de culture bactérienne et de 25 volontaires. Les milieux de culture et les cultures bactériennes de démarrage ont été préparés avant les tests sur les volontaires.
2.3.1. Culture bactérienne
Au total, 30 g de poudre de bouillon tryptone soja (TSB) ont été ajoutés à 100 ml d'eau distillée. Le mélange a été soigneusement agité jusqu'à dissolution complète de la poudre. Le volume a ensuite été ajusté avec de l'eau distillée pour atteindre un volume final de 1 l. Le milieu a ensuite été stérilisé à l'autoclave. Le milieu gélosé tryptone soja (TSA) a été préparé de manière similaire, mais avec 40 g/l de poudre de TSA.
Des cellules d'Escherichia coli (E. coli) (NCTC 10538) ont été initialement inoculées sur des plaques TSA, puis placées dans un incubateur à 37 °C pendant la nuit. Le lendemain, une colonie a été sélectionnée et transférée sur une autre plaque TSA, qui a ensuite été incubée dans les mêmes conditions. Le lendemain, une colonie a été prélevée et introduite dans 10 ml de milieu TSB. Cette culture a été incubée toute la nuit à température ambiante sous agitation. Le lendemain, la densité optique (DO) de la culture a été mesurée à l'aide d'un spectrophotomètre, puis les cellules ont été diluées dans du milieu TSB jusqu'à atteindre une DO de 0,15.
2.3.2. Application de bactéries sur l'avant-bras de volontaires
Français Cette méthode était basée sur les lignes directrices décrites dans la norme BS EN 1500:2013 [ 1 ]. Des cultures en bouillon d'E. coli avec une densité optique (DO) de 0,15 ont été systématiquement utilisées tout au long de l'expérience ; le nombre moyen d'E. coli utilisé était de 1,55 × 108 UFC/mL. Une aliquote de cette culture a été utilisée pour le dénombrement en utilisant la méthode de comptage sur plaque. Les volontaires se sont nettoyés les mains et les bras avec un savon non antibactérien, puis ont écouvillonné la zone nettoyée, qui a été placée dans 1 mL de milieu salin tamponné au phosphate (PBS) pour le dénombrement par la méthode de comptage sur plaque (servant de témoin). Une zone de 4 × 4 cm a été marquée sur la peau du volontaire pour le test. Ensuite, 100 µL de culture de nuit à DO de 0,15 ont été pipetés sur la zone de test, étalés délicatement à l'aide d'un étaleur en L et laissés sécher à l'air libre pendant 3 min.
Français Ceci a été suivi par la procédure de nettoyage en utilisant le produit de lingette comme décrit dans la section 2.1.2 . La lingette usagée a ensuite été immergée dans 10 mL de milieu neutralisant Dey-Engley (D3435, Merck, Darmstadt, Allemagne), vortexée pendant 60 s, et diluée en série deux fois avec du milieu PBS. Ensuite, 0,1 mL des bactéries a été appliqué sur une plaque de gélose pour une culture pendant la nuit et une quantification ultérieure. Après le processus d'essuyage, la surface de la zone de test de l'avant-bras a été écouvillonnée avec un écouvillon humidifié. L'écouvillon a ensuite été placé dans 1 mL de milieu PBS, et 0,1 mL a été appliqué sur une plaque de gélose pour la quantification. Des dilutions en série de pur, 10−1 et 10−2 ont été appliquées sur une plaque de gélose pour une quantification en triple. Le stock initial de bactéries a été dilué en série à 10−3, 10−4 et 10−5, puis ensemencé sur des boîtes de gélose pour le dénombrement des colonies. Pour chaque zone, le nombre d'UFC/mL a été calculé selon la formule suivante :
UFC/mL = (N ∗ DF)/VCCFU/mL = (N ∗ DF)/VC
où UFC/mL = Unité formant colonie par mL :
N = Nombre de colonies (nombre total de colonies comptées sur les plaques dans la plage optimale).
DF = Facteur de dilution (l'inverse de la dilution utilisée pour le placage).
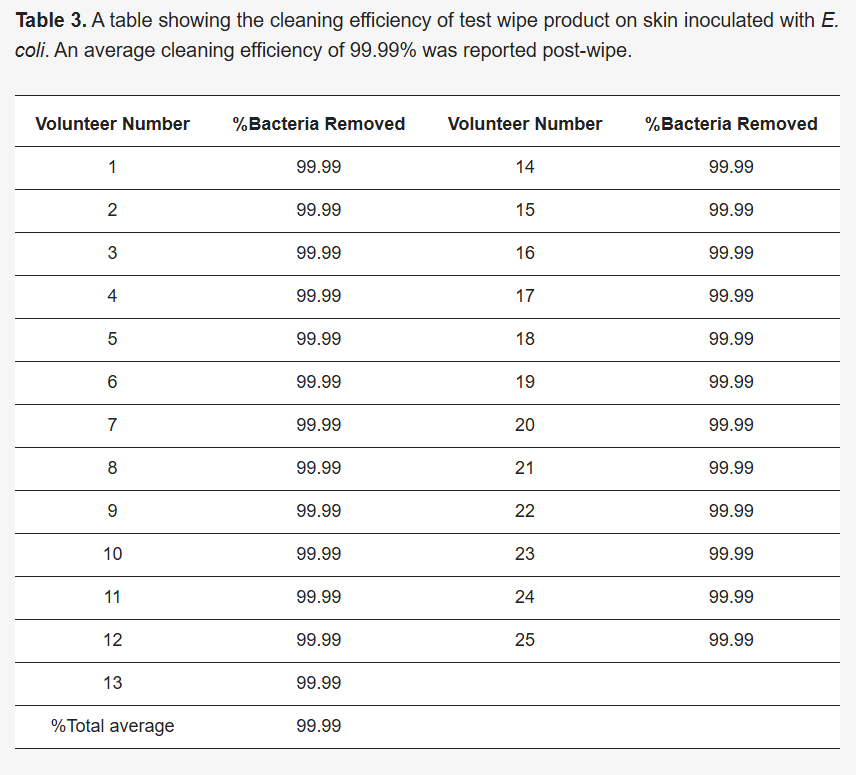
VC = Volume de culture étalé (volume de culture diluée étalée sur la gélose). Le tableau indiquant le pourcentage de bactéries éliminées se trouve à la section 3.3 ( tableau 3 ).
3. Résultats
3.1. Évaluation de l'efficacité des lingettes nettoyantes pour éliminer les matières fécales simulées (Feclone™)
La méthode Antera 3D™ adaptée a été utilisée pour évaluer l'efficacité de nettoyage des lingettes tests concernant l'élimination du Feclone™ des avant-bras de volontaires. Les résultats ont été analysés à l'aide du paramètre volumique du logiciel Antera 3D™. Le volume désigne l'épaisseur ou le volume global des résidus ou contaminants présents à la surface de la peau, et la réduction de volume après nettoyage indique une élimination réussie (voir figure 1 ). Le pourcentage d'élimination a été calculé selon la formule suivante :
𝑠𝑣0−𝑠𝑣1⁄𝑠𝑣0×100sv0−sv1∕sv0×100
où SV0 = Volume cutané (mm3) avec pré-essuyage Feclone™.
SV1 = (Volume cutané (mm3) après essuyage - volume cutané (mm3) avant application de Feclone™).
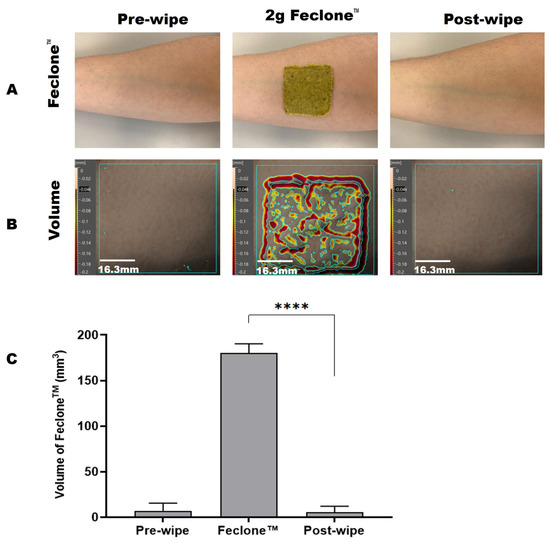
Figure 1. ( A ) Images représentatives montrant la peau humaine de l'avant-bras avant et après l'application et le retrait de Feclone™ à l'aide du produit de lingette d'essai ; l'imagerie a été réalisée à l'aide d'un appareil photo de téléphone. ( B ) Volume de Feclone™ détecté sur la surface cutanée de l'avant-bras à l'aide de la méthode Antera 3D™ et nettoyage avec le produit de lingette. La zone d'application pour l'analyse était de 40 mm × 40 mm. La barre d'échelle verticale représente le volume et la topographie de la peau, tandis que la barre d'échelle horizontale fait référence à la mesure 2D de la région cutanée définie. ( C ) Montre les volumes de peau avant l'essuyage, Feclone™ et après l'essuyage observés avec la méthode Antera 3DTM. Il a été noté que le produit de lingette réduisait l'augmentation du volume cutané induite par Feclone™ jusqu'aux niveaux avant l'application. Une analyse par test t apparié du volume cutané résiduel après administration de Feclone™ et après l'essuyage a montré une différence hautement significative (**** p < 0,0001). Le graphique a été tracé sous forme de moyenne avec écart type (SD) à l'aide de GraphPad Prism 10 (GraphPad Software, 225 Franklin Street, Fl. 26, Boston, MA 02110, États-Unis). Cela représente une efficacité de nettoyage moyenne de 100,92 %.
3.2. Évaluation du produit de nettoyage sur les pores de la peau humaine
Une réduction des paramètres des pores tels que le nombre total de pores, le volume et la surface des pores a été observée après avoir essuyé la peau de l'avant-bras du volontaire avec le produit de nettoyage ( Figure 2 ).
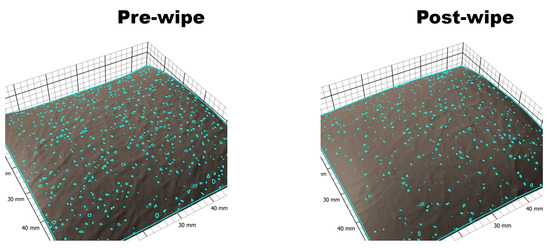
Figure 2. Une image représentative du logiciel Antera 3DTM montrant la réduction observée des pores cutanés détectables (nombre, surface totale, volume total) après nettoyage avec un produit de nettoyage.
3.3. Évaluation de l'efficacité des lingettes nettoyantes pour éliminer E. coli
L'efficacité des lingettes pour éliminer la contamination bactérienne a également été évaluée. Le nombre d'UFC/mL a été calculé pour chaque zone, puis les moyennes ont été déterminées. Ces résultats indiquent que les lingettes ont éliminé efficacement 99,99 % des cellules bactériennes et nettoyé efficacement les zones cutanées contaminées. Ceci a été validé par la collecte des lingettes usagées pour quantification bactérienne après nettoyage, ainsi que par un écouvillonnage de la zone propre pour culture sur plaques TSA (voir Figure 3 A, B).
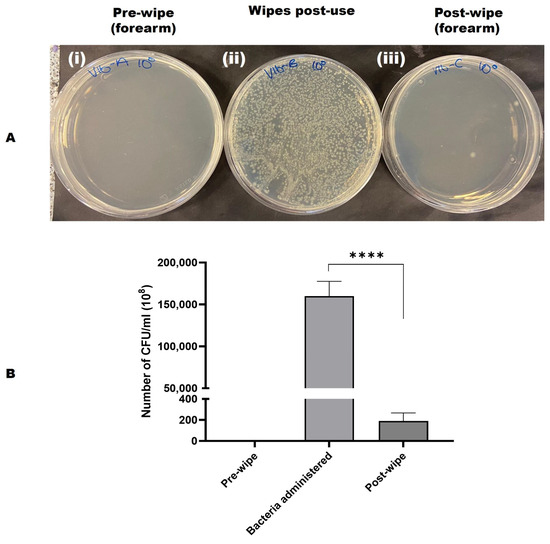
Figure 3. ( A ) Une image représentative montrant l'efficacité d'élimination bactérienne des lingettes de test sur la peau humaine contaminée. ( i ) Écouvillon pré-essuyage plaqué ( ii ) Lingette usagée plaquée ( iii ) Écouvillon post-essuyage plaqué. V = volontaire, A = échantillon pré-essuyage, B = Lingette post-utilisation, C = échantillon post-essuyage, 100 = échantillon pur/non dilué. ( B ) Graphique de l'efficacité d'élimination bactérienne du produit de lingette en utilisant E. coli et le comptage microbiologique. Il a été observé que les lingettes de test avaient une élimination bactérienne de 99,99 % de ce qui a été administré. L'analyse du test t apparié des bactéries administrées et du comptage post-essuyage a montré une différence très significative (**** p < 0,0001). Le graphique a été tracé comme moyenne avec écart type (SD) à l'aide de GraphPad Prism 10. V = volontaire, A = échantillon avant essuyage, B = essuyage après utilisation, C = échantillon après essuyage, 100 = échantillon pur/non dilué.
4. Discussion
Français Cette étude visait à concevoir et évaluer une méthode alternative pour réaliser des études d'efficacité de nettoyage de produits de lingettes en utilisant une caméra Antera 3D™, un appareil d'imagerie et d'analyse dermique. Des lingettes pour bébé disponibles dans le commerce (WaterWipes®) ont été utilisées dans cette étude et ont été testées pour leur efficacité de nettoyage avec des matières fécales synthétiques (Feclone™) et des E. coli contaminants de la surface cutanée des avant-bras de volontaires. La caméra Antera 3D™, un outil d'évaluation de produits cosmétiques validé [ 11 ], a été utilisée dans de nombreuses études cosmétiques telles que celles impliquant la quantification des rides, de l'acné et de la pigmentation [ 11 , 18 , 19 ], et donc une adaptation de la norme européenne BS EN 1500:2013 [ 1 ] intégrant la caméra Antera 3D™ pour l'évaluation quantitative et qualitative de l'efficacité de nettoyage des lingettes a été développée et testée en utilisant le produit de lingette. L'analyse objective du test FecloneTM a utilisé le paramètre de volume du logiciel pour fournir une évaluation approfondie de l'efficacité de nettoyage des lingettes.
Français Les résultats de l'évaluation visuelle et de l'analyse par caméra Antera 3D™ ont démontré que cette méthode était appropriée pour évaluer l'élimination du Feclone™ de la peau humaine à l'aide de lingettes, qui ont montré une efficacité de nettoyage du Feclone™ de 100,92 %. Nous émettons l'hypothèse que la valeur d'élimination > 100 % pourrait être due à la sensibilité de la méthode de caméra Antera 3D™ à détecter l'élimination par lingette du Feclone™ appliqué et de tout débris cutané préexistant. Une approche d'imagerie similaire pour déterminer l'efficacité de nettoyage des lingettes a été décrite par Lee et al. [ 8 ] et consiste en un ordinateur avec un scanner et un logiciel d'analyse d'images ; cependant, cette étude a été menée en utilisant un contaminant étalé sur une plaque de verre et non sur de la peau humaine. Les techniques d'imagerie offrent donc une alternative à la méthode gravimétrique traditionnelle utilisée pour évaluer l'efficacité de nettoyage des lingettes, qui a été signalée comme étant sujette à des erreurs expérimentales.
La méthode gravimétrique consiste généralement à enregistrer le poids de la lingette avant et après essuyage afin de déterminer l'efficacité du nettoyage. Cette technique se concentre sur l'analyse de la lingette et non de la surface à nettoyer. Cette méthode est sujette à des erreurs liées au processus, notamment à la manipulation des lingettes pendant la pesée, ce qui peut entraîner un transfert d'humidité de la lingette vers les gants du testeur et une inévitable évaporation de l'humidité des lingettes testées. Ces facteurs peuvent affecter les résultats obtenus et doivent être pris en compte comme variables expérimentales. Cependant, avec la méthode de caméra Antera 3D™, une approche optique, l'évaporation de l'humidité et la manipulation des lingettes sont moins préoccupantes, car l'efficacité du nettoyage est déduite directement de la surface de la peau et non de la différence de poids des lingettes. Cette méthode est donc potentiellement utile pour corriger les erreurs courantes en analyse gravimétrique. Français Les autres avantages associés aux méthodes de caméra Antera 3D™ proposées incluent sa capacité d'imagerie cutanée 3D, sa facilité d'utilisation, sa précision, sa reproductibilité et sa lecture multiple de paramètres cutanés tels que la taille des pores, les imperfections, les rides et la rugosité. Cependant, certaines limites ont été observées avec les modèles proposés, notamment l'incertitude quant à leur applicabilité dans d'autres domaines de caractérisation de l'efficacité des lingettes humides, tels que l'analyse du taux de séchage des lingettes (taux d'évaporation de l'humidité de la lingette lorsqu'elle est exposée à l'atmosphère au fil du temps), l'analyse de la captation des lingettes (capacité de la lingette humide à capter la lotion) et les études de transfert de lotion (libération de la lotion de la lingette sur la peau) [ 1 , 8 , 20 ]. Étant donné que la méthode proposée utilise un dispositif spécifique, la caméra Antera 3D™ et le logiciel associé sont nécessaires pour exécuter ou reproduire la méthode, ce qui constitue une limitation potentielle à une application généralisée. Le modèle est une technique optique avec des variables telles que la distance fixe, le degré de résolution (0,1 mm) et la bande spectrale (sept) pouvant être obtenues avec la caméra Antera 3D™, faisant de la topographie cutanée reconstruite une estimation [ 21 ]. La sensibilité de la technique proposée lui permet de détecter ce qui est présent sur la peau (cheveux, pores, sébum, cicatrices, taches de rousseur, etc.) ; cependant, cela ne devrait pas influencer ou provoquer d'artefacts dans les données générées, car le protocole stipule que les mesures de base de la peau doivent être prises en premier.
Il est intéressant de noter que le nettoyage de la peau avec les lingettes en question a eu un impact sur la réduction du nombre total moyen de pores, de leur volume et de leur surface, ce qui est d'une importance capitale, car diverses études ont démontré une relation entre un nombre de pores plus faible et une peau plus saine [ 14 , 22 , 23 ]. Ceci est probablement attribué à la combinaison de la formulation et de la composition des lingettes, où une formulation à faible tension superficielle étale et humidifie suffisamment les pores de la peau pour permettre à la lingette de les nettoyer efficacement du sébum, de la sueur et d'autres débris cellulaires. La réduction du nombre moyen de pores et de leur taille peut également être favorisée par la température plus froide des lingettes elles-mêmes. La température des lingettes semble plus froide que la température de la peau ; par conséquent, cela pourrait être la raison de la fermeture temporaire des pores. Certaines études ont rapporté que le refroidissement de la peau entraîne une réduction de la taille et du nombre de pores via une vasoconstriction cutanée et un raffermissement de la peau [ 24 , 25 , 26 ]. Français De plus, l'extrait de pépins de pamplemousse (GSE), un ingrédient revitalisant pour la peau et un ingrédient du produit de lingette utilisé, aurait des propriétés antimicrobiennes [ 27 , 28 , 29 , 30 ]. Il posséderait également une activité antioxydante et aiderait à soulager la congestion cutanée en purifiant, nettoyant et dégageant les pores obstrués pour une peau lisse et éclatante, ainsi qu'en resserrant les pores de la peau grâce à sa capacité matifiante [ 31 , 32 ]. Il est proposé que ces lingettes, WaterWipes® (WaterWipes UC, Drogheda, Irlande), pourraient être utilisées comme un moyen moins invasif de nettoyer les pores et de minimiser leur apparence, étant donné que, pris dans son ensemble, le changement dans la zone, le volume et le nombre de pores après l'essuyage pourrait être une combinaison de toutes les raisons ci-dessus ; Il s'agit toutefois d'un sujet distinct, et des recherches supplémentaires doivent être menées pour valider ces résultats et déterminer le mécanisme d'action exact, car les températures des lingettes et de la peau des volontaires n'ont pas été prises en compte dans cette étude. Néanmoins, les capacités de visualisation et de mesure des pores de la caméra Antera 3D™ (Miravex Ltd., Dublin, Irlande) ont permis de mieux comprendre l'effet des lingettes sur la peau.
5. Conclusions
En conclusion, les résultats de cette étude démontrent que la méthode de la caméra Antera 3D™ peut constituer une alternative efficace pour évaluer l'efficacité des lingettes nettoyantes. Ses avantages incluent sa simplicité d'utilisation, la reproductibilité des données, la lumière contrôlée dans la zone d'image interne et le fait qu'il s'agisse d'une unité portable offrant une haute résolution et une lecture multiparamétrique. Cependant, aucune comparaison n'ayant été effectuée avec d'autres méthodes d'évaluation de l'efficacité du nettoyage (comme la technique gravimétrique), cette technique proposée est destinée à servir d'alternative potentielle aux méthodes existantes. Les lingettes utilisées dans cette étude se sont avérées efficaces pour éliminer substantiellement Feclone™ et E. coli de la peau humaine. Des recherches complémentaires pourraient explorer les performances des lingettes sur différents types de peau et zones corporelles et dans diverses conditions environnementales afin d'élargir leur applicabilité et de mieux comprendre leur efficacité grâce à la méthode développée. Globalement, cette étude apporte des informations précieuses sur l'efficacité de la méthode de la caméra Antera 3D™ pour mesurer l'efficacité du nettoyage des lingettes nettoyantes.
Contributions des auteurs
Conceptualisation, TY, NB, JS et EG; méthodologie, AAAA, AM; KH et NB; Investigation et analyse des données, AM, KH et WS; rédaction — préparation de l'ébauche originale, WS; rédaction — révision et édition, WS, NB, JS, EG et TY; ressources, EG, JS et TY; supervision, NB et TY; administration et financement du projet, TY, EG et JS Tous les auteurs ont lu et accepté la version publiée du manuscrit.
Financement
Cette recherche a reçu un financement de WaterWipes UC.
Déclaration du comité d'examen institutionnel
Français Cet essai sur des volontaires humains a été mené conformément à la Déclaration d'Helsinki et approuvé par le Comité d'éthique de la recherche humaine de l'Université technologique de Munster (référence MTU-HREC-FER-24-004). La gouvernance du Comité d'éthique de la recherche humaine de l'Université technologique de Munster est telle que décrite dans la Politique d'éthique de la recherche humaine de l'Université [ 33 ], et est conforme à la Déclaration de politique nationale sur la garantie de l'intégrité de la recherche en Irlande (Forum national sur l'intégrité de la recherche (2019) [ 34 ]. Toute activité de recherche qui implique des êtres humains en tant que participants à la recherche doit faire l'objet d'un examen éthique formel, avant de commencer.
Déclaration de consentement éclairé
Tous les volontaires ont fourni un consentement éclairé écrit avant de participer à cette étude.
Déclaration de disponibilité des données
Toutes les données peuvent être trouvées dans cet article.
Remerciements
Tous les volontaires des deux études sont remerciés pour leur rôle dans la collecte de données.
Conflits d'intérêts
Les auteurs Jill Sommerville et Emer Gilligan étaient employés par la société WaterWipes UC. Les autres auteurs déclarent que la recherche a été menée en l'absence de toute relation commerciale ou financière susceptible d'être interprétée comme un conflit d'intérêts potentiel.
Références
- Cheriaa, R.; Boubaker, J. Évaluation de la qualité des lingettes humides pour bébés. J. Ind. Text. 2022 , 51, 2124S–2147S. [ Google Scholar ] [ CrossRef ]
- Visscher, M. ; Odio, M. ; Taylor, T. ; White, T. ; Sargent, S. ; Sluder, L. ; Smith, L. ; Flower, T. ; Mason, B. ; Rider, M. ; et al. Soins cutanés chez les patients en USIN : effets des lingettes par rapport au tissu et à l'eau sur l'intégrité de la couche cornée. Néonatologie 2009 , 96, 226–234. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Garcia Bartels, N. ; Massoudy, L. ; Scheufele, R. ; Dietz, E. ; Proquitté, H. ; Wauer, R. ; Bertin, C. ; Serrano, J. ; Blume-Peytavi, U. Programme d'entretien standardisé des couches : étude pilote prospective randomisée sur la fonction de barrière cutanée et l'IL-1α épidermique chez les nouveau-nés. Pediatr. Dermatol. 2012 , 29, 270–276. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Rodriguez, KJ ; Cunningham, C. ; Foxenberg, R. ; Hoffman, D. ; Vongsa, R. La science derrière les lingettes humides pour la peau des nourrissons : analyse des ingrédients, sécurité et efficacité. Pediatr. Dermatol. 2020 , 37, 447–454. [ Google Scholar ] [ CrossRef ]
- Odio, M. ; Streicher-Scott, J. ; Hansen, RC Lingettes jetables pour bébé : efficacité et douceur cutanée. Dermatol. Nurs. 2001 , 13, 107–112, 117–118, 121. [ Google Scholar ]
- Ehretsmann, C. ; Schaefer, P. ; Adam, R. Tolérance cutanée des lingettes pour bébé chez les nourrissons atteints de dermatite atopique, et comparaison de la douceur des lingettes et de l'eau sur la peau des nourrissons. J. Eur. Acad. Dermatol. Venereol. 2001 , 15, 16–21. [ Google Scholar ] [ CrossRef ]
- Blume-Peytavi, U. ; Lavender, T. ; Jenerowicz, D. ; Ryumina, I. ; Stalder, J. ; Torrelo, A. ; Cork, MJ. Recommandations issues d'une table ronde européenne sur les meilleures pratiques en matière de soins cutanés sains pour les nourrissons. Pediatr. Dermatol. 2016 , 33, 311–321. [ Google Scholar ] [ CrossRef ]
- Lee, J. ; Kim, S. ; Oh, KW. Analyse d'images : une nouvelle technique pour déterminer l'efficacité des chiffons d'essuyage. Fibres Polym. 2006 , 7, 73–78. [ Google Scholar ] [ CrossRef ]
- Kandil, SM ; Soliman, II ; Diab, HM ; Bedair, NI ; Mahrous, MH ; Abdou, EM. Transporteurs vésiculaires de phosphate d'ascorbyle de magnésium pour administration topique ; préparation, évaluation in vitro et ex vivo, optimisation factorielle et évaluation clinique chez les patients atteints de mélasma. Drug Deliv. 2022 , 29, 534–547. [ Google Scholar ] [ CrossRef ]
- Prendergast, P.M. Imagerie cutanée en médecine esthétique. Dans Médecine esthétique : Art et techniques ; Prendergast, P.M., Shiffman, M.A., éd. ; Springer : Berlin/Heidelberg, Allemagne, 2012 ; p. 59–68. ISBN 978-3-642-20113-4. [ Google Scholar ]
- Messaraa, C. ; Metois, A. ; Walsh, M. ; Hurley, S. ; Doyle, L. ; Mansfield, A. ; O'Connor, C. ; Mavon, A. Mesure des rides et de la rugosité par l'Antera 3D et son application à l'évaluation des produits cosmétiques. Skin Res. Technol. 2018 , 24, 359–366. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Francesco, A. Étude clinique prospective randomisée d'une nouvelle formulation topique pour la réduction des rides du visage et la régénération dermique. J. Cosmet. Dermatol. 2021 , 20, 2832–2840. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Anqi, S.; Xiukun, S.; Ai'e, X. Évaluation quantitative des peaux sensibles par ANTERA 3D® associé à GPSkin Barrier®. Skin Res. Technol. 2022 , 28, 840–845. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Parvar, SY ; Amani, M. ; Shafiei, M. ; Rastaghi, F. ; Hosseini, SA ; Ahramiyanpour, N. Efficacité et effets indésirables des traitements pour les pores du visage : article de synthèse. J. Cosmet. Dermatol. 2023 , 22, 763–775. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- WaterWipe. Notre histoire de lingettes pour bébé | WaterWipes UK. WaterWipes. Disponible en ligne : https://www.waterwipes.com/uk/en/our-story (consulté le 12 juillet 2024).
- Marsh, RG ; Miller, KH ; Dannenberg, A. Méthode d'évaluation de l'adhérence des salissures ou des exsudats à la peau. US20100228107A1, 9 septembre 2010. Disponible en ligne : https://patents.google.com/patent/US20100228107A1/en (consulté le 3 juillet 2024).
- Jubinville, E.; Girard, M.; Trudel-Ferland, M.; Fliss, I.; Jean, J. Inactivation de norovirus murins en suspension dans la matière organique simulant les conditions réelles de contamination virale. Food Environ. Virol. 2021 , 13, 544–552. [ Google Scholar ] [ CrossRef ]
- Araco, A.; Araco, F. Étude préliminaire prospective et randomisée comparant un polynucléotide hautement purifié à un placebo dans le traitement des cicatrices d'acné modérées à sévères. Aesthet. Surg. J. 2021 , 41, NP866–NP874. [ Google Scholar ] [ CrossRef ]
- Niemeyer-van der Kolk, T. ; Buters, TP ; Krouwels, L. ; Boltjes, J. ; de Kam, ML ; van der Wall, H. ; van Alewijk, DCJG ; van den Munckhof, EHA ; Becker, MJ ; Feiss, G. ; et al. L'omiganane, un peptide antimicrobien topique, corrige la dysbiose cutanée, mais n'améliore pas les symptômes cliniques chez les patients atteints de dermatite atopique légère à modérée dans un essai contrôlé randomisé de phase 2. J. Am. Acad. Dermatol. 2022 , 86, 854–862. [ Google Scholar ] [ CrossRef ]
- Hossain, MM ; Jones, JM ; Dey, S. ; Carr, GJ ; Visscher, MO. Quantification du transfert de lotion des lingettes pour bébé sur la peau des prématurés et des nouveau-nés. Food Chem. Toxicol. 2015 , 84, 106–114. [ Google Scholar ] [ CrossRef ]
- Gitlina, Y. ; Guarnera, GC ; Dhillon, DS ; Hansen, J. ; Lattas, A. ; Pai, D. ; Ghosh, A. Mesure pratique et reconstruction de la réflectance spectrale cutanée. Graphique. Forum 2020 , 39, 75–89. [ Google Scholar ] [ CrossRef ]
- Messaraa, C. ; Metois, A. ; Walsh, M. ; Flynn, J. ; Doyle, L. ; Robertson, N. ; Mansfield, A. ; O'Connor, C. ; Mavon, A. Capacités 3D d'Antera pour la mesure des pores. Skin Res. Technol. 2018 , 24, 606–613. [ Google Scholar ] [ CrossRef ]
- Vachiramon, V. ; Namasondhi, A. ; Anuntrangsee, T. ; Kositkuljorn, C. ; Jurairattanaporn, N. Étude de l'association d'ultrasons microfocalisés et d'acide hyaluronique pour le traitement des pores dilatés du visage chez les Asiatiques. J. Cosmet. Dermatol. 2021 , 20, 3467–3474. [ Google Scholar ] [ CrossRef ]
- Shahzad, Y. ; Louw, R. ; Gerber, M. ; du Plessis, J. Briser la barrière cutanée par modulation de température. J. Control. Publication 2015 , 202, 1–13. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Johnson, JM ; Kellogg, DL. Contrôle thermique local de la circulation cutanée humaine. J. Appl. Physiol. 2010 , 109, 1229–1238. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Charkoudian, N. Débit sanguin cutané dans la thermorégulation chez l'adulte : fonctionnement, dysfonctionnement et raisons. Mayo Clin. Proc. 2003 , 78, 603–612. [ Google Scholar ] [ CrossRef ] [ PubMed ]
- Park, H.-K.; Kim, S.-B. Activité antimicrobienne de l'extrait de pépins de pamplemousse. Korean J. Food Nutr. 2006 , 19, 526–531. [ Google Scholar ]
- Sung-Hwan, CHO ; Il-Won, SEO ; Jong-Duck, C. ; In-Saeng, JOO. Activité antimicrobienne et antioxydante de l'extrait de pamplemousse et de pépins sur les produits de la pêche. Korean J. Fish. Aquat. Sci. 1990 , 23, 289–296. [ Google Scholar ]
- Jong-Duck, C. ; Il-Won, SEO ; Sung-Hwan, CHO. Études sur l'activité antimicrobienne de l'extrait de pépins de pamplemousse. Korean J. Fish. Aquat. Sci. 1990 , 23, 297–302. [ Google Scholar ]
- Saaty, AH. Activité antibactérienne et antivirale des extraits de pépins de pamplemousse : impact du coronavirus 2 sur le syndrome respiratoire aigu sévère. Arch. Pharm. Pract. 2022 , 13, 68–73. [ Google Scholar ] [ CrossRef ]
- Khaiat, A. ; Saliou, C. Extraits botaniques. Dans Cosméceutiques et cosmétiques actifs, 3e éd. ; CRC Press : Boca Raton, Floride, États-Unis, 2015. [ Google Scholar ]
- Yarovaya, L. ; Waranuch, N. ; Wisuitiprot, W. ; Khunkitti, W. Étude clinique des modifications cutanées chez les Asiatiques après application d'une formule de protection solaire contenant de l'extrait de pépins de raisin. J. Cosmet. Dermatol. 2022 , 21, 4523–4535. [ Google Scholar ] [ CrossRef ]
- MTU. Politique d'éthique de la recherche sur les êtres humains de la MTU. Disponible en ligne : https://www.mtu.ie/media/mtu-website/governance/policies-and-publications/academic-council-poli-cies-and-regulations/research-innovation-and-postgraduate-study/Human_Research_Ethics_Policy_AC_app_030622.pdf (consulté le 16 juillet 2024).
- Wood, K. Déclaration de politique nationale sur la garantie de l'intégrité de la recherche en Irlande. Disponible en ligne : https://www.iua.ie/publications/national-policy-statement-on-ensuring-research-integrity-in-ireland/ (consulté le 5 septembre 2024).
Avis de non-responsabilité/Note de l'éditeur : Les déclarations, opinions et données contenues dans toutes les publications sont uniquement celles des auteurs et contributeurs individuels et non celles de MDPI et/ou du ou des éditeurs. MDPI et/ou le ou les éditeurs déclinent toute responsabilité pour toute blessure aux personnes ou aux biens résultant des idées, méthodes, instructions ou produits mentionnés dans le contenu.
© 2024 par les auteurs. Licencié MDPI, Bâle, Suisse. Cet article est en libre accès et distribué selon les termes et conditions de la licence Creative Commons Attribution (CC BY) ( https://creativecommons.org/licenses/by/4.0/ ).
More on the Skincare Hub
View allPeau sèche vs peau déshydratée : quelle est la différence et comment en prendre soin ?
Quelle est la différence et comment en prendre soin ?

Érythème fessier
L’érythème fessier est un problème courant chez les bébés, et pour les jeunes parents, il est souvent très angoissant de voir son tout-petit souffrir ou être irrité. Heureusement, il existe des solutions pour prévenir et soulager l’érythème fessier. Je réponds ici à certaines des questions les plus fréquentes à ce sujet, et j’espère que mes réponses vous seront utiles pour prendre soin de votre bébé. – Dr Alexis Granite